
研究背景:
糖尿病骨缺损愈合障碍是高血糖与慢性炎症交互作用导致的严重并发症,其病理机制涉及ROS过量积累、AGEs形成、成骨-成脂分化失衡及血管生成受损等多重微环境紊乱。当前治疗策略主要依赖功能化支架或细胞因子递送,但存在材料稳定性差、释放行为不可控及难以协同调控复杂病理网络等局限。
气体治疗尤其是一氧化氮(NO)因其组织渗透性强及抗炎-促血管双重生物活性成为研究热点:NO可通过NF-κB/MAPK通路抑制炎症反应并驱动M2型巨噬细胞极化,同时经sGC/cGMP/PKG信号级联增强血管新生。然而,糖尿病状态下内源性NO合成途径受损,而外源性NO递送体系普遍存在突释效应明显、生物半衰期短及时空可控性不足等缺陷,无法满足慢性骨修复对长期精准调控的需求。因此,开发兼具病理微环境动态响应与NO可控长效释放功能的一体化支架体系,成为突破糖尿病骨再生治疗瓶颈的关键方向。

针对上述问题,深大罗永祥/国科大阮长顺团队提出通过“物理限域”策略主动调控NO生成反应空间,实现由突释向持续、自调节释放模式的转变。基于此构建了一种用于骨植入的微孔限域长效NO释放支架(MP-LAS),采用3D打印结合相分离技术制备PCL/水凝胶壳-核结构。其微孔结构作为扩散屏障限制L-Arg外泄,仅允许外界H2O2向内扩散并在限域空间内与L-Arg反应生成NO,从而实现“扩散限域响应释放”。同时,核心ROS响应性水凝胶在高ROS糖尿病环境下选择性降解,清除过量氧化应激,实现ROS清除与持续NO释放的协同调控。该体系通过免疫调节、促血管生成和促进成骨的多重协同作用,逆转糖尿病病理循环,重建有利于骨再生的微环境;外层PCL结构则提供力学支撑与结构稳定性,并通过表面微孔调控降解行为。该策略不仅为糖尿病骨缺损修复提供了一种可转化的新方案,也为复杂病理条件下实现分子精准时空调控释放建立了新的设计范式。该文章于2026年2月24日以《Micropore-Confined ROS-Responsive 3D-Printed Shell-Core Scaffolds for Long-Term NO Release to Orchestrate Immunomodulation and Angiogenesis in Diabetic Bone Defect Repair》为题发表于《Advanced Materials》上(DOI: 10.1002/adma.202521475)。

研究示意图. MP-LAS支架的示意图,该支架具有ROS响应性持续释放NO的功能,可用于修复糖尿病骨缺损。
(1)MP-LAS支架的制备与表征
MP-LAS支架采用3D打印构建PVA/SA水凝胶核心,并通过TSPBA交联赋予ROS响应性。外层通过溶液浸涂法形成PCL壳层,并引入樟脑作为致孔剂构建贯通微孔结构(图 1A)。当PCL:樟脑质量比为1:1时,表面形成有序多孔结构,孔隙率为57 ± 9%,显著高于2:1与1:2组(图 1B–C);对照组(1:0)仅形成1–5 μm的表面非贯通微孔。1:1组孔径分布集中,平均孔径为20.2 ± 9.8 μm,约50%孔径位于15–25 μm区间,90%分布于10–50 μm范围(图 1D)。SEM显示PCL壳层内外表面均存在开放性微孔,截面可见厚度为85 ± 12 μm的均一壳层及贯通孔道结构(图 1E)。该双向开放孔结构形成连续互联网络。掺入nHA后,壳层仍保持均一微孔结构(图 1F),EDS证实Ca与P元素均匀分布(图 1G)。光学显微镜显示支架保持规则宏观孔结构及打印丝间距,PCL层均匀包覆水凝胶核心(图 1H)。结果表明,该方法实现了完整壳-核结构及均一微孔限域体系的构建。

图1.微孔限域壳核支架的表征。(A) PCL微孔壳的制备示意图。(B) 不同PCL/樟脑质量比制备的壳核支架表面微孔的SEM图像。(C) 不同PCL/樟脑比例下支架表面的孔隙率。(D) PCL/樟脑比例为1:1时支架表面的孔径分布。(E) PCL壳内外表面以及壳核纤维横截面的SEM图像。(F) 显示整体微孔形貌的代表性图像。(G) MP-LAS支架的EDS Ca/P元素分布图。(H) 支架的光学显微镜和SEM图像(无PCL壳的水凝胶支架(HS)、无孔PCL支架(LAS)、微孔支架(MP-LAS))。
(2)MP-LAS支架的体外性能评价
MP-LAS支架中的水凝胶通过TSPBA与PVA形成硼酸酯动态共价键,在ROS环境下发生氧化断裂并逐步降解(图 2A)。在H₂O₂条件下,MP-LAS核心水凝胶完全降解,仅保留微孔PCL壳层;去离子水中结构保持稳定。无孔壳层的LAS在H₂O₂中未发生水凝胶降解(图 2B)。抗氧化实验显示,MP-LAS对H₂O₂、DPPH和O₂•⁻的清除率分别为77%、73%和69%,均高于LAS组(图 2C)。Griess法检测表明,HS组30天内完成突释(t₁/₂=6天);LAS组NO释放低于1 µM;MP-LAS实现持续释放超过90天,半衰期为18天(图 2D)。NO释放行为可通过调节PCL:樟脑比例、L-Arg负载量及外源H₂O₂浓度实现调控(图 2E)。体外降解结果显示,HS于27 ± 4天内完全降解;LAS在90天内质量损失约20%;MP-LAS持续降解至第90天并转变为贯通空腔PCL结构(图 2F)。力学测试结果表明,LAS的抗压强度(0.7 ± 0.03 MPa)和杨氏模量(0.98 ± 0.04 MPa)高于HS(0.4 ± 0.04 MPa;0.52 ± 0.04 MPa);MP-LAS较LAS分别下降约23%和22%,但仍高于HS(图 2G)。
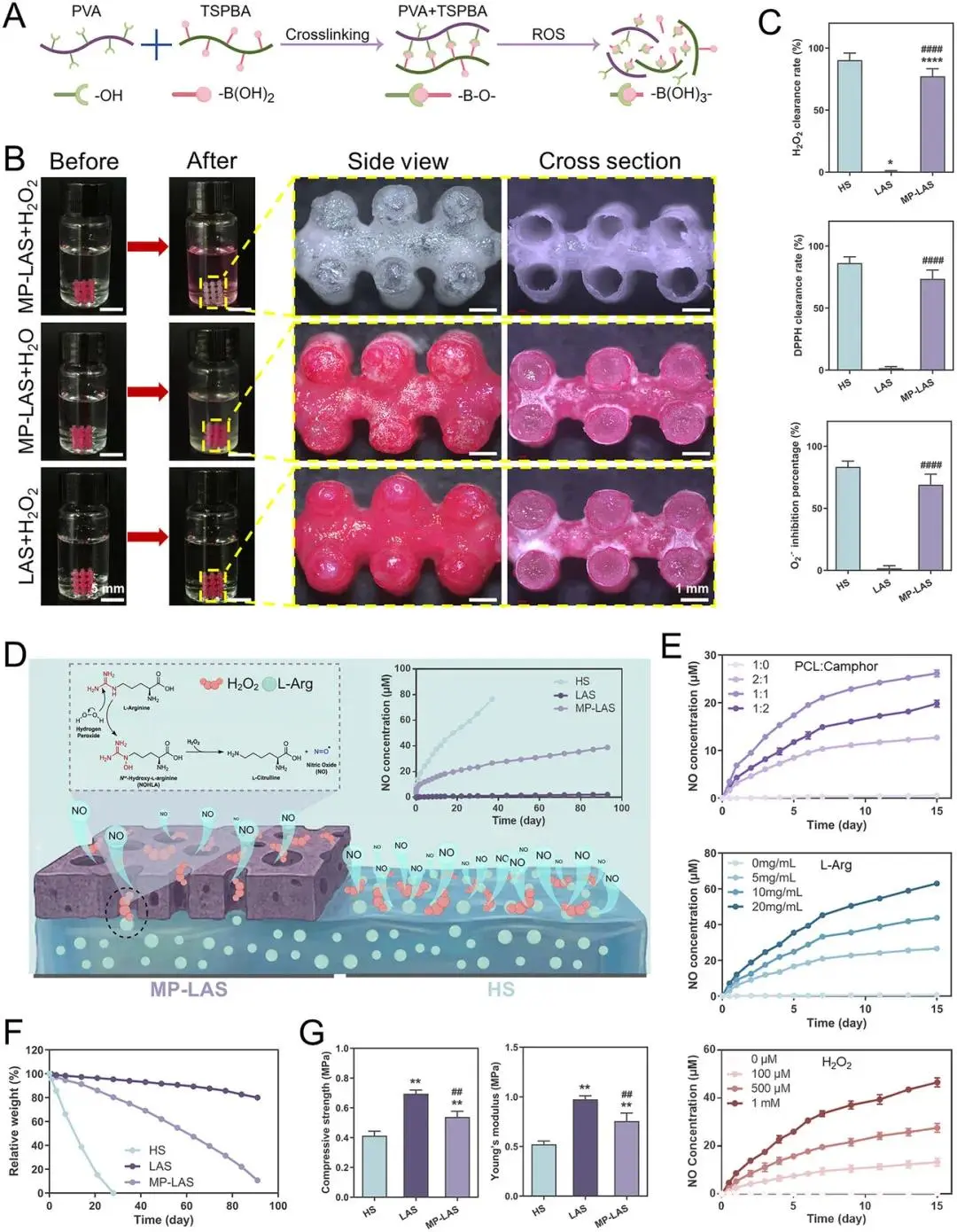
图2.支架的体外性能。(A) ROS响应性水凝胶反应过程示意图。(B) 支架ROS响应行为的评估(1 M H2O2,7天)。(C) 支架的抗氧化性能:对H2O2、DPPH自由基和超氧阴离子(O2•− )的清除能力。(D) 水凝胶支架(HS)突释和微孔核壳支架(MP-LAS)控释的示意图比较,以及NO生成机制和90天NO释放曲线。(E) NO释放曲线:通过调节PCL:樟脑比例、L-精氨酸浓度和H2O2浓度实现对NO释放的控制。(F) 支架的体外降解曲线。(G) 支架的力学性能:抗压强度、杨氏模量。
(3)MP-LAS支架的抗氧化和抗炎能力评估
细胞相容性结果表明,L-Arg浓度低于10 mg/mL无明显细胞毒性。MP-LAS支架具有良好生物相容性并支持细胞黏附与增殖,而NO突释的HS组表现出明显细胞毒性。DAF-FM DA荧光染色显示MP-LAS组细胞内NO绿色荧光显著增强(图 3A),Griess法检测培养基中NO水平显著升高(图 3C),表明NO在ROS刺激下产生并进入细胞。DCFH-DA检测显示MP-LAS显著降低BMSCs内ROS水平(图 3B),H₂O₂定量结果显示其降低约48%(图 3D)。JC-1染色结果显示,H2O2刺激导致线粒体膜电位下降,MP-LAS干预后绿色荧光强度较H2O2组降低约6倍,红/绿荧光比恢复至正常对照组的88 ± 5%(图 3E)。qRT-PCR结果显示,MP-LAS上调SOD2和CAT基因表达1.8倍和2.2倍(图 3F)。巨噬细胞极化分析表明,MP-LAS降低iNOS+(M1型)比例并提高Arg-1+(M2型)比例(图 3H)。ELISA结果显示TNF-α和IL-6水平降低,IL-10和TGF-β水平升高(图 3I)。qRT-PCR及Western blot结果呈一致趋势(图 3J–L),表明MP-LAS调控炎症相关因子表达。

图3.评估MP-LAS支架的抗氧化和抗炎能力。(A) 使用NO特异性荧光探针DAF-FM DA检测NO释放(未负载L-精氨酸的微孔支架(MPS))。(B) 使用ROS敏感荧光探针DCFH-DA评估ROS清除能力(NC:不含H2O2的正常条件)。( C) 细胞培养上清液中的NO浓度。(D)细胞培养上清液中的H2O2浓度。(E) JC-1荧光图像显示BMSCs的正常(红色)和去极化(绿色)线粒体膜电位。 ( F) 通过qRT-PCR评估细胞中抗氧化酶基因(SOD2、CAT)的表达。(G) 支架介导的免疫调节机制示意图。(H) 使用免疫荧光染色分析巨噬细胞(Raw264.7)表型标志物。 (I) 采用ELISA法检测促炎细胞因子(TNF-α、IL-6)和抗炎细胞因子(IL-10、TGF-β)的表达水平。(J) 采用qRT-PCR法评估巨噬细胞中炎症相关基因(TNF-α、IL-10)的表达。(K) 采用Western blot法检测巨噬细胞中炎症相关蛋白(TNF-α、IL-6)的表达。(L) 采用Western blot法定量分析巨噬细胞中炎症相关蛋白(TNF-α、IL-6)的表达。柱状图的背景颜色代表实验条件:浅粉色代表H2O2环境,浅蓝色代表无H2O2的正常条件。
(4)MP-LAS支架血管成骨潜能的评估
划痕实验显示,在ROS条件下LAS组HUVECs迁移率为30 ± 4%,MPS组为50 ± 6%,MP-LAS组达到88 ± 7%并接近完全愈合(图 4A,B);Transwell实验结果一致。Matrigel成管实验表明,MP-LAS组形成更致密连续的血管网络,总管长和分支点数量分别为LAS组的约3.5倍和4倍(图 4C–E)。在高ROS条件下,BMSCs迁移能力下降,MPS和MP-LAS均显著促进迁移,MP-LAS效果最明显(图 4F,G)。ALP活性和ARS染色结果显示,LAS组ALP活性和钙结节形成最低;MPS和MP-LAS显著提高ALP活性及钙沉积水平,MP-LAS高于MPS(图 4H–K)。转录组分析显示,MP-LAS组差异表达基因显著增加(图 4L),KEGG富集提示cGMP–PKG及PI3K–Akt信号通路显著激活,GO分析富集于“血管发育”等条目。qPCR及Western blot结果显示,MP-LAS组VEGF、HIF-1α、RUNX2和OCN在mRNA和蛋白水平均显著上调(图 4M),提示其促进血管生成与成骨相关基因表达(图 4N)。

图4.MP-LAS支架血管成骨潜能的评估。(A) HUVECs划痕愈合实验12小时的代表性图像,以及(B)迁移率的定量分析。(C) HUVECs培养10小时后的管状网络形成,以及相应血管生成参数的定量评估,包括(D)管状网络总长度和(E)分支点数量。(F) BMSCs Transwell迁移实验24小时,以及(G)细胞迁移的定量分析。(H) BMSCs第14天的ALP染色,以及(I)ALP活性的定量分析。(J) BMSCs第14天的ARS染色,以及(K)矿化结节形成的定量分析。 (L)对来自 LAS 和 MP-LAS 组的 HUVEC 进行 RNA-seq 分析,包括转录组分析中差异表达基因的火山图和热图、基因本体论 (GO) 通路分析中富集程度最高的 30 个条目(分别包含 10 个生物过程、10 个细胞组分和 10 个分子功能条目)以及 KEGG 通路分析中富集程度最高的 20 个条目。(M)与血管生成(VEGF、HIF-1α)和成骨(RUNX2、OCN)相关的基因的相对表达量。(N)示意图展示了支架释放的 NO 如何通过 sGC/cGMP/PKG 通路促进细胞内血管生成-成骨偶联。
(5)糖尿病小鼠模型皮下血管化的评估
在糖尿病小鼠皮下植入模型中,术后1周超声成像显示MP-LAS组周围新生血管数量明显多于LAS和MPS组;至第3周,各组均可见血管生成,但MP-LAS组血管密度显著更高,为LAS组的3.7倍,且血管分布于支架周边及内部区域(图5B,C)。MPS组血管生成水平亦高于LAS组(图5B,C)。组织学结果显示,MP-LAS组在支架-宿主界面形成连续新生结缔组织层,并富含CD31阳性管状结构;3周时丝间区域被新生组织填充并含有大量成熟微血管(图5D)。MPS组仅形成不连续组织层并伴有少量血管,LAS组组织反应较弱。定量分析表明,MP-LAS组血管数量为LAS组的3.3倍(图5E)。
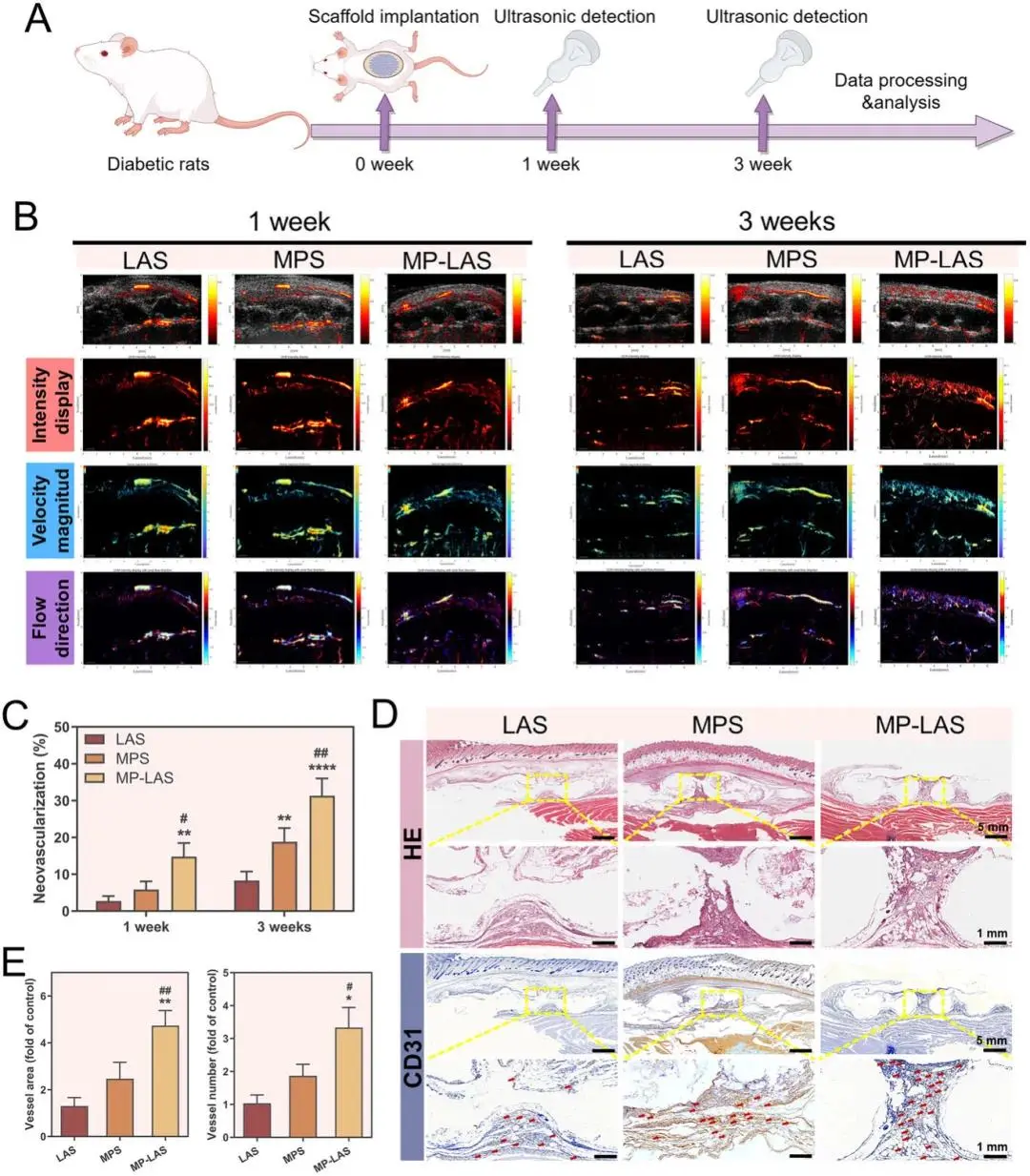
图5.利用糖尿病小鼠皮下植入模型,对支架的促血管生成能力进行体内评价。(A) 糖尿病小鼠皮下血管生成试验示意图。(B) 支架植入区域的超声血管造影:平滑强度、血流速度和血流方向。(C) 支架内及周围新生血管的定量分析。(D) 支架植入区域的代表性H&E染色和CD31免疫组化染色。(E) 血管半定量分析:血管面积和血管数量。
(6)糖尿病颅骨缺损模型中骨再生的体内评价
在高脂饮食联合STZ诱导的糖尿病大鼠5 mm颅骨缺损模型中,Micro-CT结果显示术后4周和8周MP-LAS组新骨自缺损边缘向中心呈放射状生长(图 6B),其BV/TV和BMD显著高于LAS和MPS组。术后12周,MP-LAS组BV/TV和BMD分别达到35 ± 3%和0.33 ± 0.03 g/cc,约为LAS组的2–3倍(图 6C)。组织学染色显示,MP-LAS组4周时即出现明显新生血管及类骨组织形成,12周时形成连续骨桥;LAS组缺损区以纤维组织为主,新骨形成有限(图 6D–F)。免疫荧光结果显示,MP-LAS组TNF-α阳性表达降低69%,TGF-β表达提高4倍(图 6G,H)。术后4周CD31阳性面积达35 ± 5%,显著高于LAS组(7 ± 3%)和MPS组(13 ± 4%),且与HIF-1α共定位。OPN阳性区域主要分布于缺损边缘,并与OCN及CD31阳性血管呈共表达和空间耦合分布,提示血管生成与成骨过程协同发生(图 6G,H)。

图6.糖尿病大鼠颅骨缺损模型中骨再生的评估。(A) 实验设计和治疗时间线示意图。(B) 植入后4周和12周颅骨缺损的代表性三维重建显微CT图像。(C) 骨体积/组织体积比(BV/TV)和骨密度(BMD)的定量分析。(D) 苏木精-伊红(H&E)染色和马松三色染色的代表性图像。(E) 12周时支架和新生组织面积的百分比。(F) 12周时马松三色染色新生骨面积百分比的定量分析。(G) 炎症标志物(TGF-β,黄色)、血管生成标志物(HIF-1α,红色)和成骨标志物(OPN,绿色)的免疫荧光组织化学染色。(H) 免疫荧光染色中TGF-β、HIF-1α和OPN阳性区域的定量分析。
(7)糖尿病大鼠股骨缺损实验
在糖尿病大鼠股骨缺损模型中,Micro-CT结果显示术后4、8及12周MP-LAS组新骨形成最为显著,而LAS组缺损区域持续存在(图7A)。术后12周,MP-LAS组BV/TV(41 ± 3% vs. 20 ± 5%)、BMD(0.66 ± 0.07 g/cc vs. 0.32 ± 0.08 g/cc)、Tb.N(0.92 ± 0.07 mm-1 vs. 0.52 ± 0.08 mm-1)显著高于LAS组,Tb.Sp(0.30 ± 0.03 mm vs. 0.63 ± 0.03 mm)显著降低(图 7B)。组织学结果显示,4周时MP-LAS组缺损边缘已出现新生骨及胶原纤维;12周时形成致密新骨并表现出良好结构连续性,MPS组修复程度低于MP-LAS组(图7C)。体内安全性评估显示未见明显毒性反应。免疫荧光结果显示,4周时MP-LAS组H型血管标志物(EMCN/CD31)阳性面积显著高于MPS和LAS组,新生血管密度增加(图7D,E)。MP-LAS组TNF-α阳性面积降低,TGF-β表达升高。成骨相关标志物阳性面积较对照组提高2–4倍(图 7D,E)。

图7.糖尿病大鼠股骨缺损模型中的骨再生。(A) 股骨缺损的代表性三维重建显微CT图像。(B) 骨参数的定量分析:骨体积/组织体积比(BV/TV)、骨密度(BMD)、骨小梁数量(Tb.N)和骨小梁间距(Tb.Sp)。(C) 缺损区域的代表性苏木精-伊红(H&E)染色和马松三色染色。(D) 炎症标志物(TNF-α,黄色)、H型血管标志物(EMCN,绿色/CD31,红色)和成骨标志物(OCN,绿色)的免疫荧光组织化学染色。(E) 免疫荧光染色中EMCN、CD31、TNF-α和OPN阳性区域的定量分析。数据以均值±标准差( n =3)表示。
本研究构建了一种基于“微孔物理限域”策略的长效NO释放支架系统,通过微孔PCL壳层与负载L-Arg的ROS响应性水凝胶核协同,实现了局部、可控、持续超过3个月的NO释放。 该结构通过物理限域反应界面,将释放机制由传统的“被动扩散与爆发式释放”转变为“扩散调控下的按需供给”,显著降低高剂量毒性风险,并赋予系统对ROS水平变化的自适应响应能力。在糖尿病病理微环境中,该系统优先清除过量ROS、恢复氧化还原稳态,同时触发持续NO生成,协同发挥抗炎、促血管生成及促成骨作用,促进血管-成骨耦合修复。体内外实验结果证实,ROS清除与持续NO释放的协同效应是增强血管化骨再生的关键机制。该闭环调控体系可在病理信号升高时增强治疗输出,在微环境改善后自动下调释放速率,实现动态平衡与长期安全性。 该研究不仅验证了MP-LAS支架在糖尿病骨缺损修复中的显著疗效,也提出了一种通过多尺度结构工程主动编程生化反应时空进程的生物材料设计范式,为复杂病理环境下的精准组织再生提供了新的技术路径。

|
创赛生物 提供高品质的医疗产品和服务 |
联系我们 |
产品中心 |
扫码关注
关注公众号 扫码加客服
|

