
研究背景:
水凝胶生物粘合剂因其卓越的生物相容性和可调节的物理化学特性,已被广泛应用于伤口护理、人机界面和植入式生物电子设备。尽管这些粘合剂在加速伤口愈合方面表现出临床效用,但仅用单一材料同时恢复受损皮肤的组织结构和感觉功能仍是一项重大挑战。作为一种灵活且耐用的界面,水凝胶生物粘合剂能够感知人体运动和生理线索,有效模拟皮肤的体感功能。关键是,它同时支持皮肤生物电子学中的伤口愈合和多信号监测。

针对上述问题,陕西科技大学生物质与功能材料研究所王学川教授、党旭岗副教授报道了一种可注射自愈多功能生物质基水凝胶生物粘合剂,采用羧甲基壳聚糖(CMCS)、丝胶蛋白(SS)和天然保湿因子(NMF)作为原料,实现皮肤生物电子与再生伤口愈合的综合管理。水凝胶生物粘合剂表现出显著的溶胀能力(1094.46%),组织渗出物的快速吸收,以及显著的止血效能。与此同时,水凝胶生物胶对温度、应力应变和生物电信号表现出高度敏感,能够有效检测各种人体运动和温度预警。值得注意的是,水凝胶生物粘合剂具有可调调模量,精确匹配伤口部位皮肤组织的机械性能,促进伤口近乎完全愈合,并在14天内显著降低促炎因子水平。该研究于2026年1月21日以《Injectable Self-Healing Biomass-Based Hydrogel Bioadhesive Integrating Skin Bioelectronics and Regenerative Wound Healing》为题发表于《Advanced Functional Materials》(DOI:10.1002/adfm.202530332)。
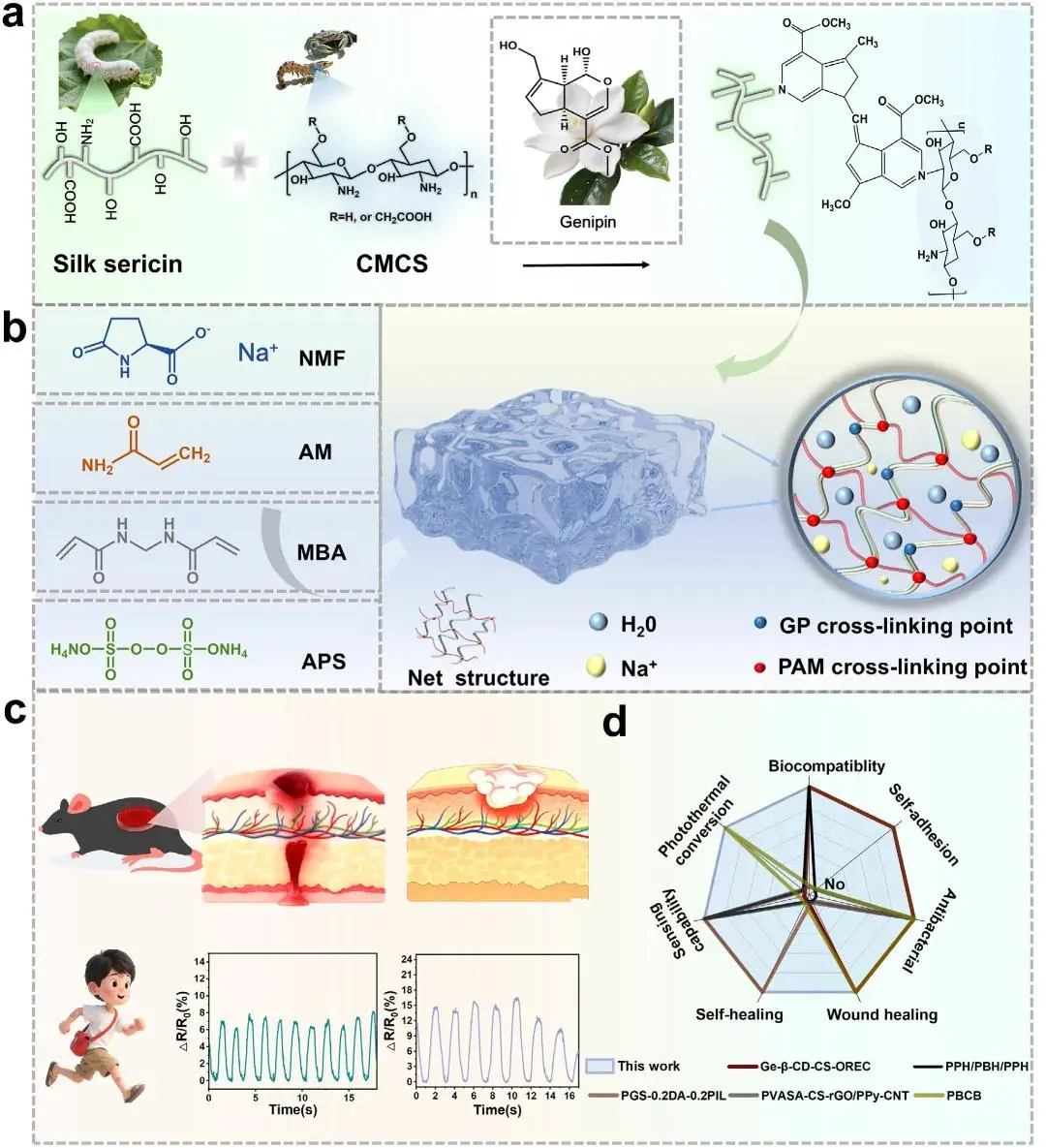
方案1. 生物质基水凝胶生物粘合剂(CMCS@SS)用于伤口修复与生物电子整合的制备示意图。
(1)CMCS@SS的结构表征
CMCS@SS双网络水凝胶的结构与性能表征表明,CMCS与SS比例显著影响材料微观形貌与热力学性质。SEM显示CMCS@SS-1形成孔径30±5 μm的均匀多边形孔结构,CMCS@SS-2因双网络动态平衡形成孔径40±8 μm的高孔隙海绵结构并呈现分级粗糙度,CMCS@SS-3则出现15-50 μm的宽分布孔径及纳米突起。FT-IR证实CMCS羧基/羟基与SS酰胺基团间存在多重氢键,酰胺I带左移至1671-1685 cm⁻¹,且高SS比例诱导β-折叠结构重构增强。XPS显示CMCS@SS-2中C 1s谱在289.0 eV出现C=C-N与-COO⁻耦合新峰,N 1s峰右移0.2 eV至399.8 eV,证实-NH₂与-C=O/-COO⁻间形成氢键和静电作用,且Na⁺信号显著增强。TGA-DSC结果表明CMCS@SS-2在主分解阶段(200-400°C)热稳定性最优,残碳率达41%,玻璃化转变温度随SS含量增加而升高。
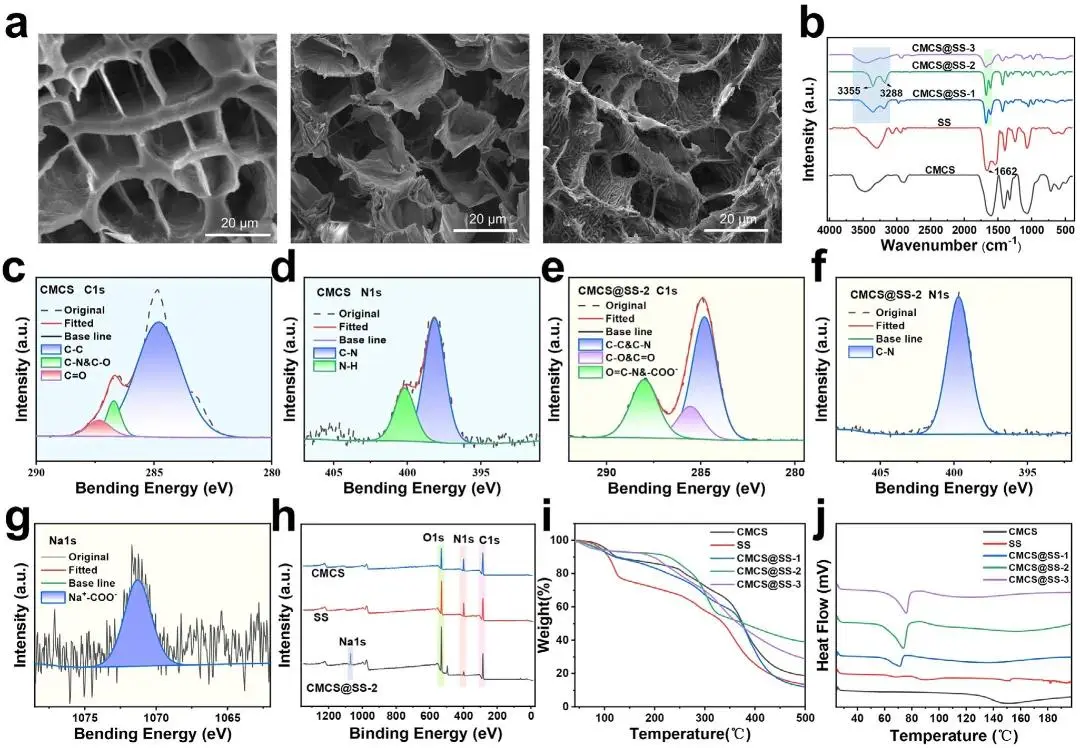
图1. CMCS@SS的形貌与结构表征。(a)CMCS@SS-1/-2/-3的SEM图像;(b)CMCS、SS和CMCS@SS的FT-IR光谱;(c,d)CMCS的XPS C 1s和N 1s谱;(e–g)CMCS@SS-2的XPS C 1s、N 1s和Na 1s谱;(h)CMCS、SS和CMCS@SS的XPS全谱;(i)CMCS、SS和CMCS@SS的TGA曲线;(j)CMCS、SS和CMCS@SS的DSC曲线。
(2)CMCS@SS的机械性能、自愈合性能、可注射性、溶胀性能与导电性
GP与CMCS/SS溶液中的-NH₂发生亲核开环反应,初期破坏物理交联网络导致体系液化,随后逐步建立三维共价交联桥,AM自由基聚合进一步固化形成双网络结构。力学性能显示SS含量增加使应变和韧性提升至1194.8%和673.62 KJ/m³,高CMCS比例则赋予204.4 kPa拉伸强度和84.89 kPa弹性模量;150%应变循环测试中传感器滞后26.4%,能量耗散435 kJ/m³。流变频率扫描证实G'高于G'',CMCS@SS-2在690%应变时G''与G'匹配,800%应变时结构失效,1%应变下可完全恢复初始模量,室温1分钟实现自愈合。可注射性测试表明预凝胶态具备足够流动性,完全交联后获得显著机械强度;剪切变稀行为证实其适用于微创递送。溶胀实验显示CMCS@SS-2在去离子水、PBS和SBF中32小时溶胀比分别为948.43%、1094.46%和988.06%,PCA-Na驱动水合膨胀,GP交联网络与PAM二次增强协同维持结构稳定性。电化学阻抗谱显示CMCS@SS-1/-2/-3内阻依次为582.12、441.68和416.23 Ω,电子电导率分别为0.0324、0.0419和0.0448 S/cm,离子迁移率分别为7.61×10⁻⁵、9.84×10⁻⁴和4.16×10⁻⁴ cm²/(V·s),CMCS@SS-2呈现最优导电性能。
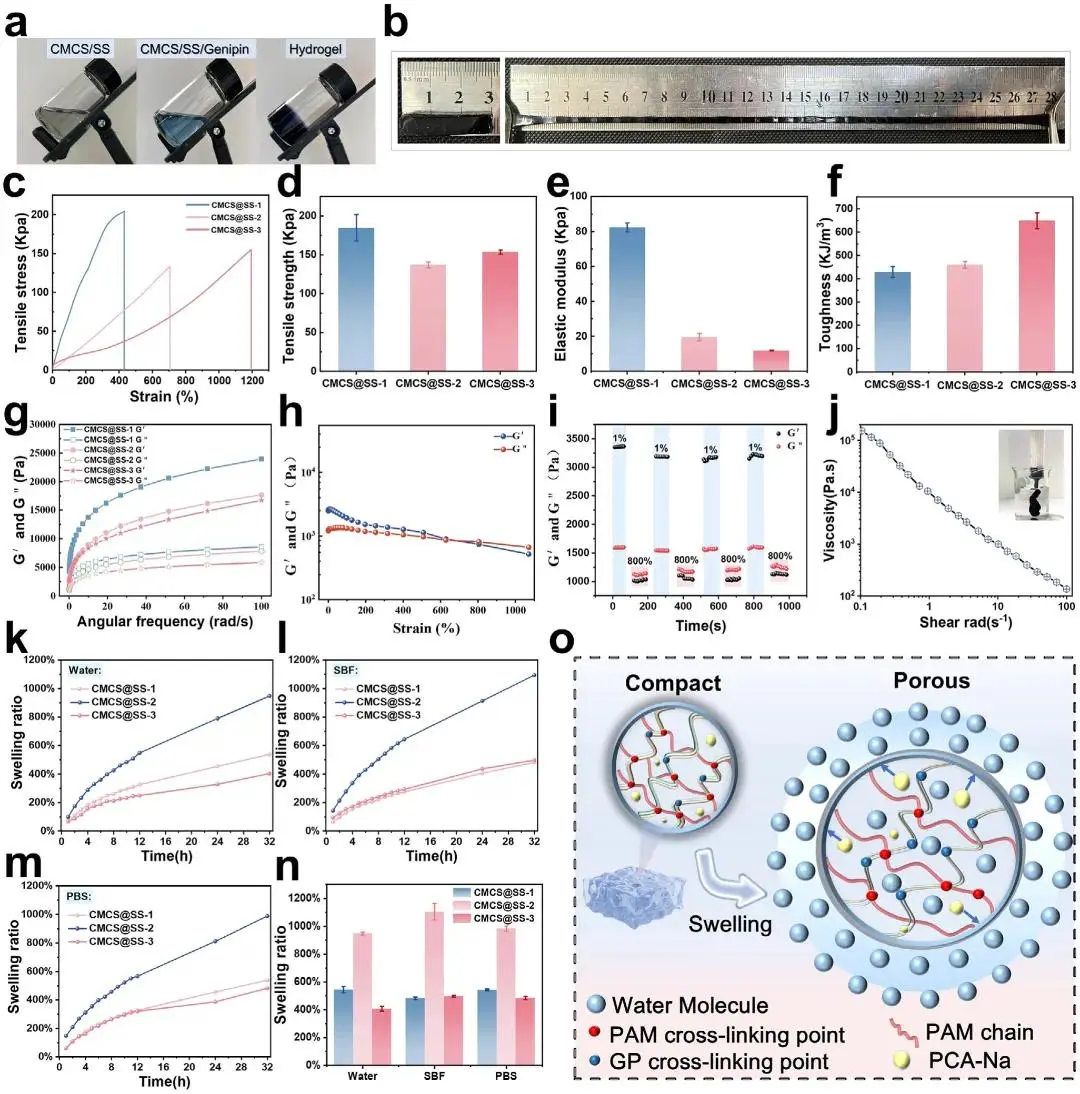
图2. CMCS@SS的制备与性能表征。(a)CMCS@SS制备示意图;(b)CMCS@SS拉伸至930%应变时的照片;(c)CMCS@SS的拉伸应力-应变曲线;(d)CMCS@SS的最大拉伸强度;(e)CMCS@SS的弹性模量;(f)CMCS@SS的韧性;(g)CMCS@SS从0.1至100 rad·s⁻¹的频率依赖性;(h)CMCS@SS的应变扫描测试;(i)通过在1%和800%交替应变下测试CMCS@SS的自愈合分析;(j)剪切速率扫描测试说明CMCS@SS的剪切变稀特性;(k)CMCS@SS在水中的时间依赖性溶胀率;(l)CMCS@SS在SBF中的时间依赖性溶胀率;(m)CMCS@SS在PBS中的时间依赖性溶胀率;(n)CMCS@SS的最大溶胀率;(o)溶胀机制示意图。
(3)CMCS@SS的生物粘附性能
CMCS@SS-2对金属、塑料、玻璃、橡胶及生物组织(皮肤、心脏、肌肉、肝脏、胃、肾脏)均表现出强粘附性,在弯曲和扭转机械变形下无边缘翘起或分层。猪皮肤搭接剪切试验显示其最大剪切强度达6.8 kPa,源于CMCS羧基与SS氨基的等摩尔比离子键合,该交联机制降低界面损伤敏感性并增强接触面积;CMCS@SS-1因SS含量不足、CMCS@SS-3因聚集诱导脆化导致粘附性能下降。粘附机制涉及酰胺/羧基与基材表面羟基的氢键作用、羧基/酚羟基与生物组织亲核物种(胺、硫醇、羟基)的共价键合,以及质子化氨基/羧基与金属离子的配位相互作用。
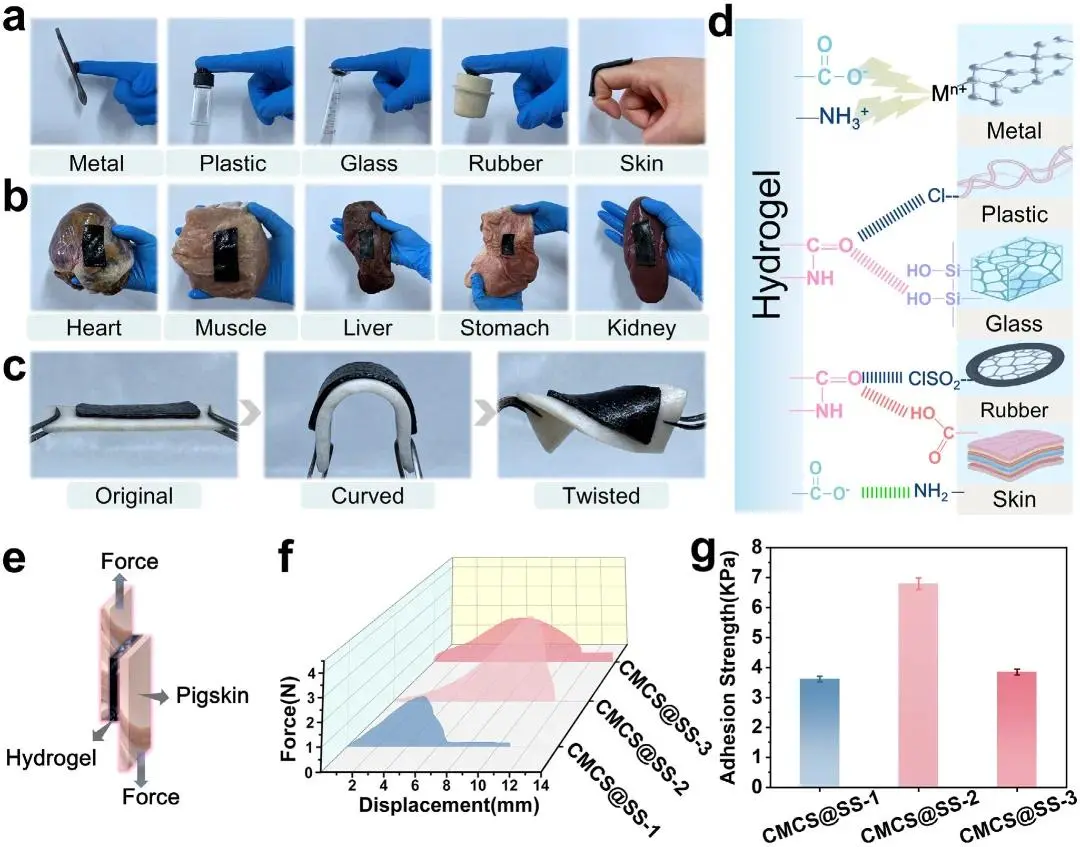
图3. CMCS@SS的粘附性能。(a,b)不同材料表面的粘附行为照片;(c)CMCS@SS对猪皮的粘附性能;(d)CMCS@SS对各种材料的粘附机制;(e)CMCS@SS猪皮粘附实验示意图;(f)CMCS@SS的粘附强度曲线;(g)CMCS@SS的最大粘附强度。
(4)CMCS@SS的光热转换性能
GP交联产生的醌结构与CMCS/SS供体-受体系统协同作用,使凝胶网络吸收980 nm近红外光触发分子内电子跃迁及非辐射弛豫,聚合物链振动与多孔结构光散射增强光捕获效率,促进光子-声子能量转换;PCA-Na通过降低氢键网络蒸发焓增强热传导,高交联密度与动态键重排确保热循环过程中的结构稳定性。红外热成像显示,2.1 W/cm²功率密度照射180 s内水凝胶表面温度从26°C升至77.3°C平台,关闭后180 s恢复至基线;六个开/关循环中峰值温度稳定在77.3-82°C区间。不同功率密度(1.2、1.5、1.8、2.1 W/cm²)下温度分别达45、57、72、77°C平台,最大温变与功率密度呈强正相关(R²=0.957)。
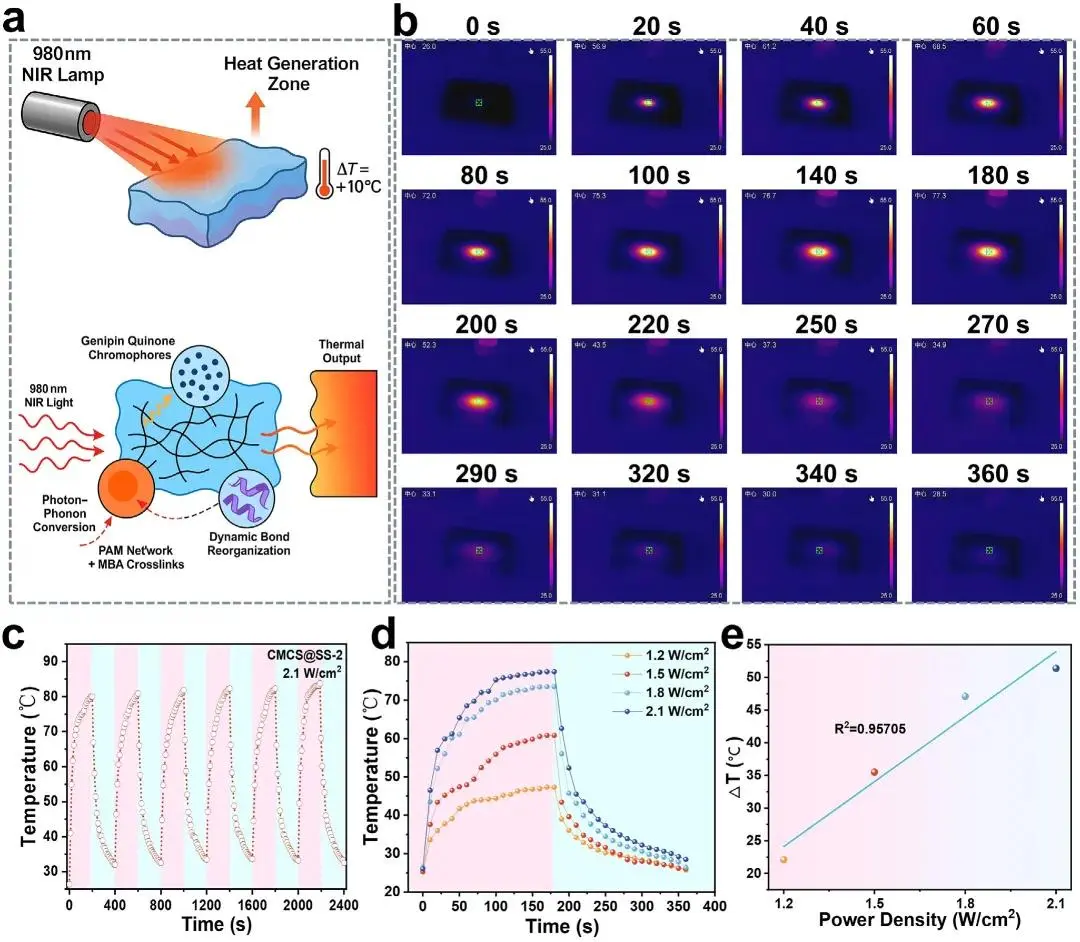
图4. CMCS@SS的光热效应。(a)980 nm红外光热效应原理;(b)2.1 W·cm⁻²功率密度980 nm NIR照射下CMCS@SS的红外热像图;(c)2.1 W·cm⁻²功率密度下6个循环辐射开/关图;(d)不同功率密度下的温度-辐射时间曲线;(e)不同功率密度980 nm NIR照射下光热转换温度与激光功率密度变化曲线的线性拟合。
(5)CMCS@SS的抗菌性能与细胞毒性分析
CMCS的质子化氨基通过静电作用结合微生物带负电荷细胞膜,破坏膜完整性并诱导内容物泄漏;SS在细菌表面形成物理保护层阻断粘附增殖,同时整合入膜脂双层改变流动性,触发膜破裂或功能损伤。抗菌实验显示,CMCS@SS-2对大肠杆菌抑菌圈最大(15.88±0.20 mm),显著高于CMCS@SS-1(12.61±0.60 mm)和CMCS@SS-3(13.58±1.05 mm);对金黄色葡萄球菌,三组抑菌圈分别为23.24±0.41、23.76±1.05和23.49±0.56 mm,该差异源于革兰氏阳性菌简单细胞壁结构与高密度磷壁酸易与CMCS结合,而革兰氏阴性菌脂多糖疏水性阻碍渗透。CCK-8试验表明CMCS@SS-2处理组1-5天细胞存活率均超98%,活/死染色未见细胞密度显著变化;1.2 W/cm²近红外照射(40-50°C,5 min)后存活率仍超98%且显著高于对照组。溶血试验显示所有浓度CMCS@SS-2溶血率均低于5%(ISO 10993-4标准),红细胞形态保持完整,上清液呈淡黄色,证实良好血液相容性。
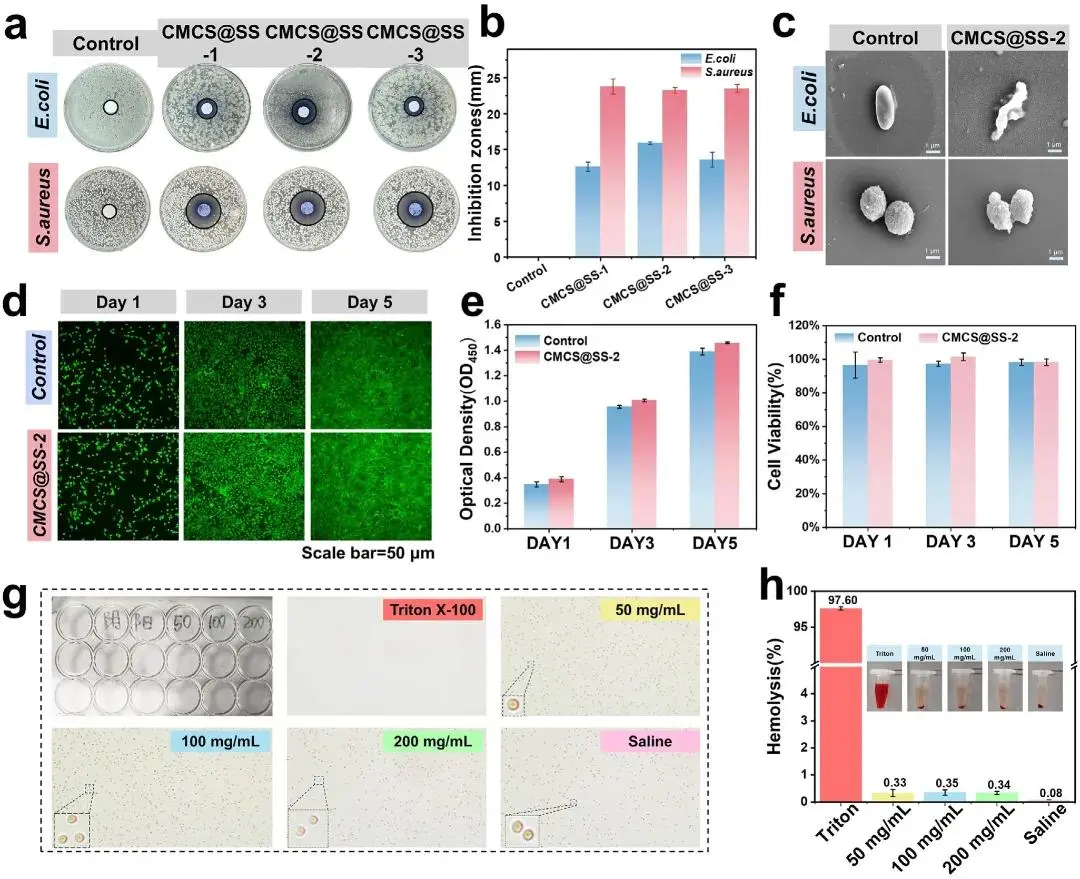
图5. CMCS@SS的抗菌性能与生物相容性。(a)CMCS@SS对大肠杆菌和金黄色葡萄球菌抑菌圈的光学图像;(b)CMCS@SS对大肠杆菌和金黄色葡萄球菌的抑菌圈直径;(c)反映细菌状态的SEM图像;(d)培养1-5天的NIH-3T3细胞活/死染色图像;(e,f)1-5天CMCS@SS的细胞活性;(g,h)CMCS@SS、生理盐水(阴性对照)和Triton X-100(阳性对照)上清液的血细胞形态和溶血分析。
(6)CMCS@SS体内伤口愈合性能的视觉检查
小鼠全层圆形伤口模型评估显示,术后第3、7、10和14天CMCS@SS-2组伤口面积持续缩小,第14天残留面积最小且闭合率达99.18%伴毛发再生;第7天闭合率显著高于未处理组和商用透明质酸敷料(Convadex 187990)对照组,第10天优势进一步扩大(p<0.01)。该效应源于CMCS@SS-2维持的湿润环境、组分协同作用及PCA-Na导电性能;CMCS的固有抗菌活性与SS促进细胞增殖、加速上皮化和抗氧化效应协同模拟天然细胞外基质,创造最佳愈合微环境。实验期间各组体重无显著差异,证实治疗安全性。
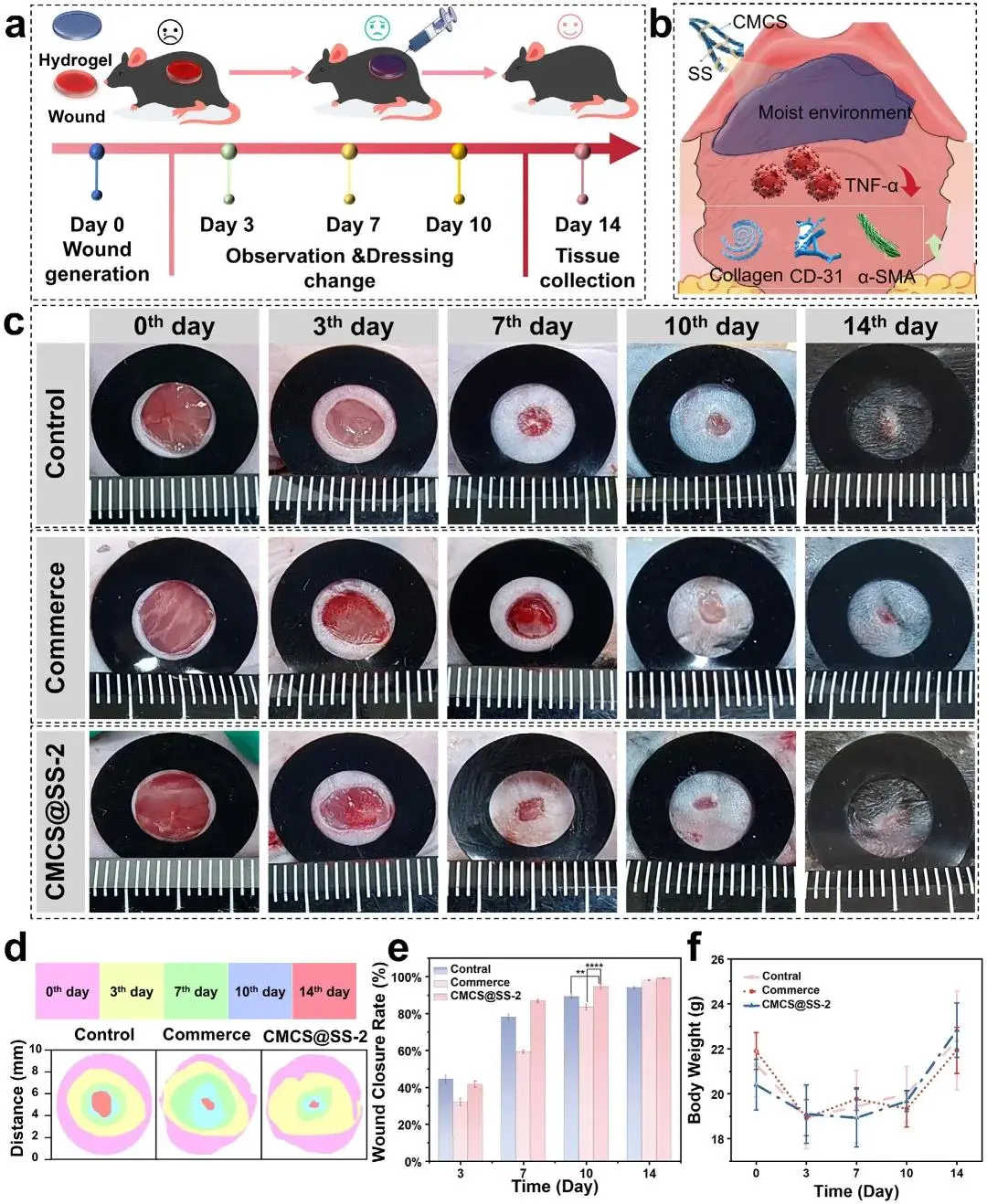
图6. CMCS@SS的体内伤口愈合评估。(a)伤口治疗手术程序示意图;(b)伤口愈合机制图;(c)愈合过程中伤口的代表性照片;(d)对照组、商用组和CMCS@SS-2组的动态伤口床演变示意图;(e)通过残留伤口面积评估的统计伤口闭合率;(f)治疗期间大鼠体重变化。
(7)伤口区域的组织学分析
第14天组织学评估显示,CMCS@SS-2组H&E染色呈现更多腺体、新生毛囊及更窄伤口宽度,Masson三色染色示广泛致密胶原纤维沉积,肉芽组织密度达87.9±1.9%且胶原呈组织化束状排列。免疫荧光定量分析表明,CMCS@SS-2组TNF-α表达显著低于对照组,源于CMCS抑制巨噬细胞过度激活及SS促进M1向M2表型极化的协同抗炎效应;CD31和α-SMA表达显著升高,证实血管生成增强与组织修复促进。机制涉及SS直接激活内皮细胞并上调促血管生成因子,CMCS三维多孔结构支撑内皮细胞迁移及管形成,其抗菌特性消除感染以营造血管生成微环境;SS驱动成纤维细胞向肌成纤维细胞分化并上调α-SMA,CMCS、SS与PCA-Na协同维持湿润环境以持续激活成纤维细胞功能,确保胶原沉积与肉芽组织成熟。
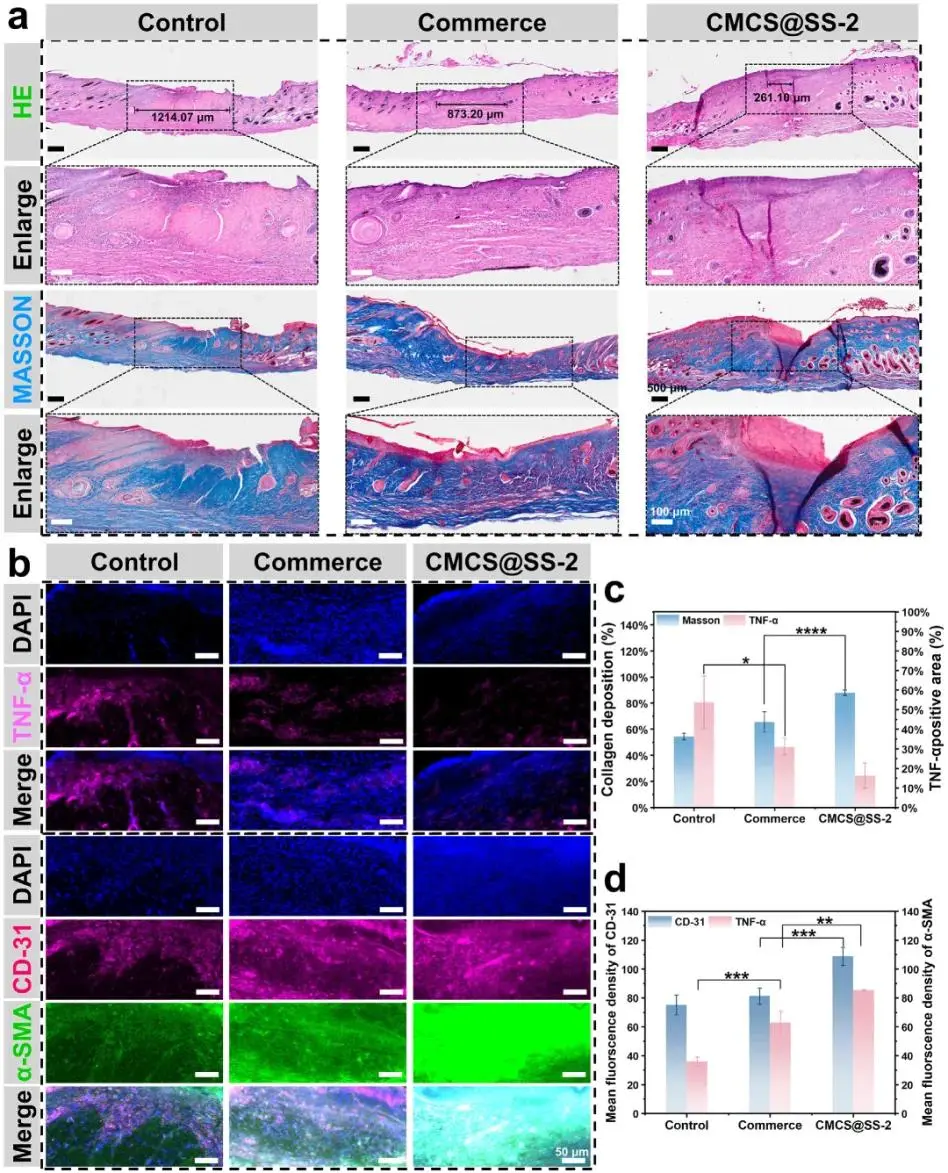
图7. 创伤组织的组织学改变及TNF-α、CD-31和α-SMA的免疫荧光分析。(a)第14天采集创伤的H&E染色和Masson三色染色组织学图像;(b)第14天对照组、商用组和CMCS@SS-2组TNF-α、CD31和α-SMA的免疫荧光图像;(c)胶原沉积统计和TNF-α免疫荧光统计;(d)CD-31和α-SMA的免疫荧光统计。
(8)应变传感与人体运动信号监测
变形后水凝胶厚度减小增强电阻,有效调节离子传输途径与动力学。CMCS@SS-2传感器在5%-175%应变范围内呈现稳定信号响应,Gauge Factor达2.24,响应时间150 ms;5%-35%应变区间反馈精确,50%-175%区间电阻变化稳定。960次循环后信号重复性优异(误差<1.5%),机械抗疲劳性良好,存在微结构松弛导致的基线漂移。贴附手指、手腕、肘部关节可准确检测运动角度,肘部曲线平坦证实信号稳定性。PBS溶胀24小时后灵敏度GF=2.26,响应时间413 ms,5%-35%小应变、50%-175%大应变及960次循环范围内均能准确捕获电阻变化。
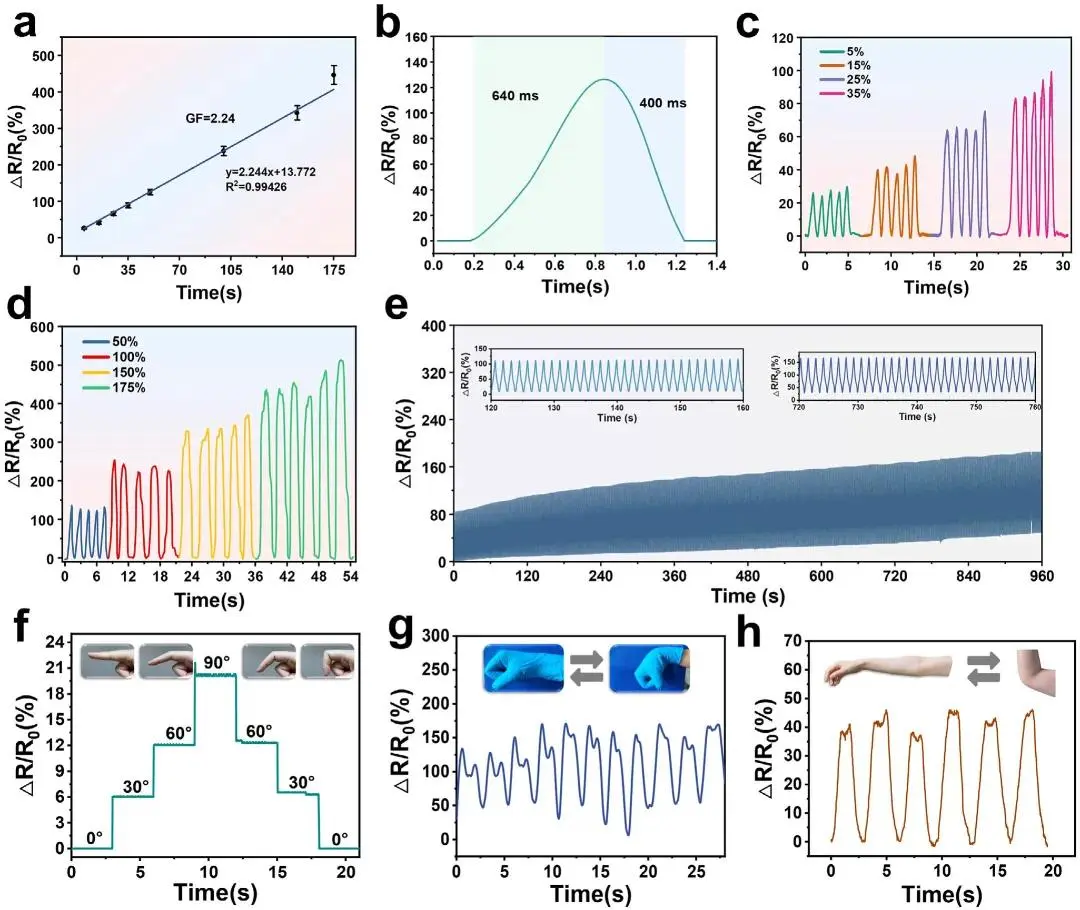
图8. CMCS@SS-2的应变传感性能。(a)拉伸应变函数的相对电阻;(b)50%应变下电信号的响应时间;(c)不同小应变下相对电阻的变化;(d)不同大应变下相对电阻的变化;(e)940次拉伸/释放循环后电传感性能的稳定性;(f)不同手指屈曲角度下相对电阻的变化;(g)不同手腕屈曲角度下相对电阻的变化;(h)肘部屈曲反映的电信号。
(9)健康监测与皮肤温度预警装置
CMCS@SS传感器网络实时监测面部肌电信号与微变形,将疼痛、神经缺陷及感染应激反应转化为客观数据,捕获皱眉、嘴角下垂等微表情动态以评估隐匿感染与神经恢复。志愿者佩戴测试显示,眉间、下巴及口罩前表面贴附可识别皱眉、恐惧、惊讶、微笑等表情,足底放置可检测摆动、行走、跑步、跳跃的电信号差异,实现关节运动状态连续监测。热敏性评估显示20°C-80°C范围呈负温度系数效应,TCR值分别为-1.96%/°C(20°C-40°C)、-2.66%/°C(40°C-70°C)、-9.79%/°C(70°C-80°C);生理温度范围(36°C-40°C)TCR值为-8.21%/°C(36°C-37.2°C)、-3.22%/°C(37.4°C-39°C)、-6.21%/°C(39°C-40°C),具备精细温度检测能力。假手指接触实验证实温度降低时电阻减少趋缓,与负热敏性一致,移除后信号快速恢复,体现高灵敏度与可逆性。
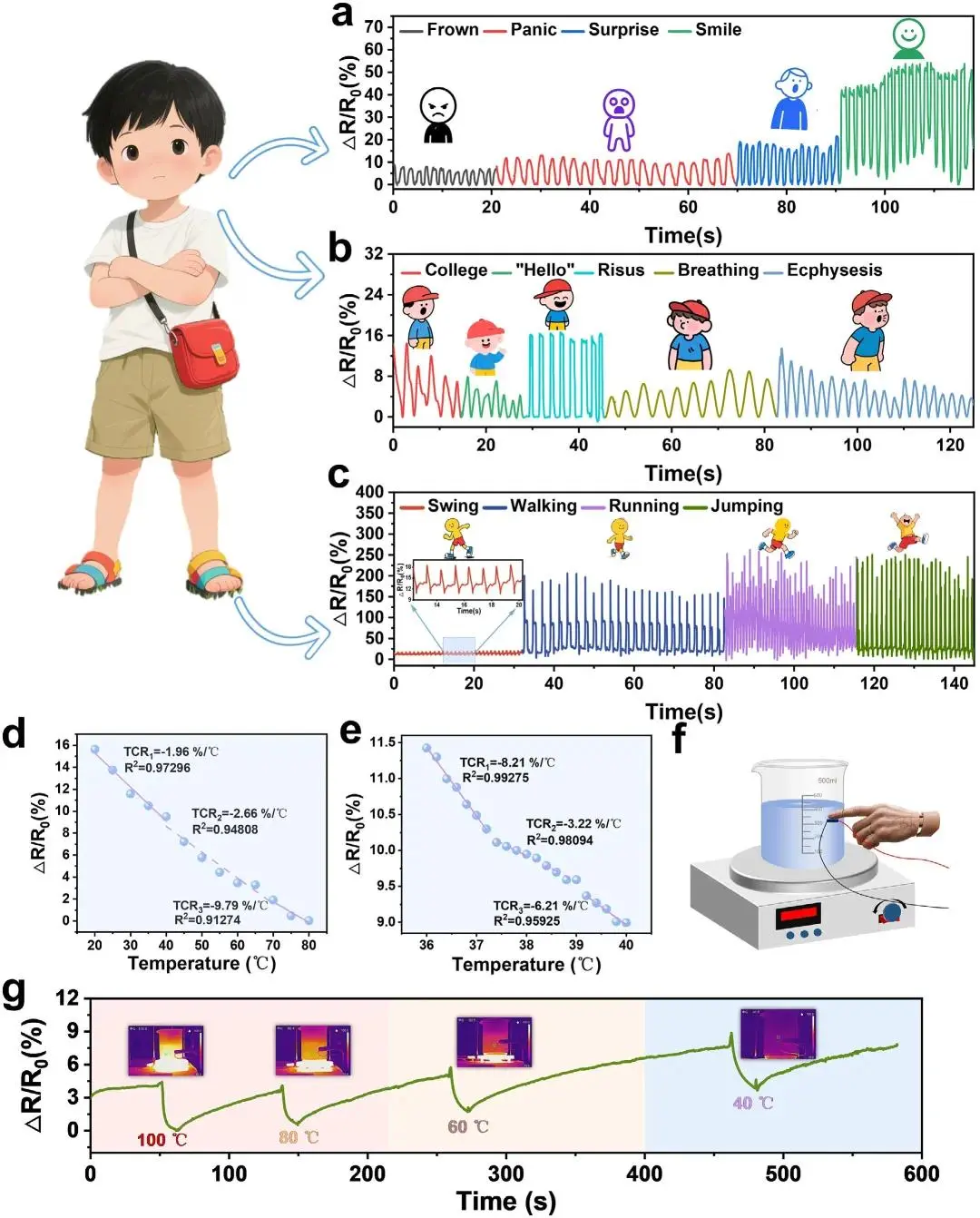
图9. 作为多功能可穿戴设备的CMCS@SS,用于监测对外部刺激(包括人类情绪、声音信号和身体运动)的实时相对电阻变化。(a)人类情绪;(b)声音信号;(c)身体运动;(d)20°C-80°C范围内负相对电阻随温度的变化;(e)36°C-40°C范围内负相对电阻随温度的变化;(f)皮肤触摸温度预警装置示意图;(g)使用加热台作为热源实现CMCS@SS对不同温度的高保真温度感觉。
本研究通过仿生交联策略构建了一种全天然生物质基双网络水凝胶粘合剂,它融合了可注射成型、力学适配、自发修复、光热抗菌、高效溶胀、生物传感与促进愈合等多重功能,为实现“粘附-抗菌愈合-电生理传感”一体化的智能伤口诊疗提供了具有潜力的材料平台。

|
创赛生物 提供高品质的医疗产品和服务 |
联系我们 |
产品中心 |
扫码关注
关注公众号 扫码加客服
|

