
心肌梗死(MI)是由于冠状动脉血流骤减或中断,导致心肌缺血、坏死,进而引发心功能下降甚至心力衰竭(HF)的严重心血管疾病。随着人口老龄化,HF的患病率持续上升,已成为重大公共卫生问题。尽管再灌注治疗是MI的主要手段,但其并发症不可预测,且缺血-缺氧、氧化应激和炎症反应会加剧心肌损伤和心室重构。因此,亟需开发能同时促进血管再生、抑制炎症与氧化应激的新型治疗策略。

针对上述问题,四川大学生物工程学院的王云兵团队设计了一种负载去铁胺(DFO)和卡维地洛(Carvedilol)的GelMA/HASH水凝胶(GelMA/HASH@DPDCNs),兼具生物相容性与可注射性。通过体外实验验证其控释性能、抗炎、抗氧化及促血管生成作用,并进一步在大鼠MI模型中证实该水凝胶可通过协同促进血管新生与抑制炎症反应,有效改善心肌梗死后的心功能,为MI治疗提供新思路。该文章于2025年7月21日以《An injectable hydrogel loaded with deferoxamine and carvedilol for the treatment of acute myocardial infarction》为题发表于《Chemical Engineering Journal》(DOI:10.1016/j.cej.2025.166294)。
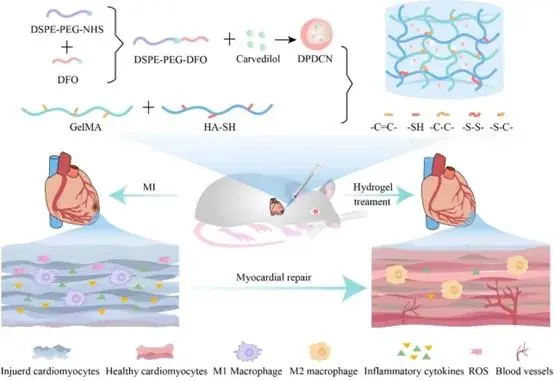
研究示意图
(1) 水凝胶的制备与表征
图1A-B的1H NMR分别显示GelMA在5.5与5.7 ppm出现甲基丙烯酸酯峰、HASH于2.5 ppm出现胱胺二甲烯峰,证实两者合成完成。图S3与1C的TEM显示DPNNs及DPDCNs呈球形;图S4与1D的DLS表明载药后粒径由107 nm增至约200 nm。图S7与1E的SEM显示Hydrogel 1与4孔径均>100 μm,DPDCNs引入未破坏多孔结构。图1F应变扫描示两凝胶在540 %应变内G′>G″,呈凝胶态;图1G-H释放曲线:卡维地洛72 h累计释放≈44.7 %,10 d达81.3 %;DFO 72 h累计释放≈31.8 %,14 d达62.8 %,实现早期快速释药与后期持续释药。
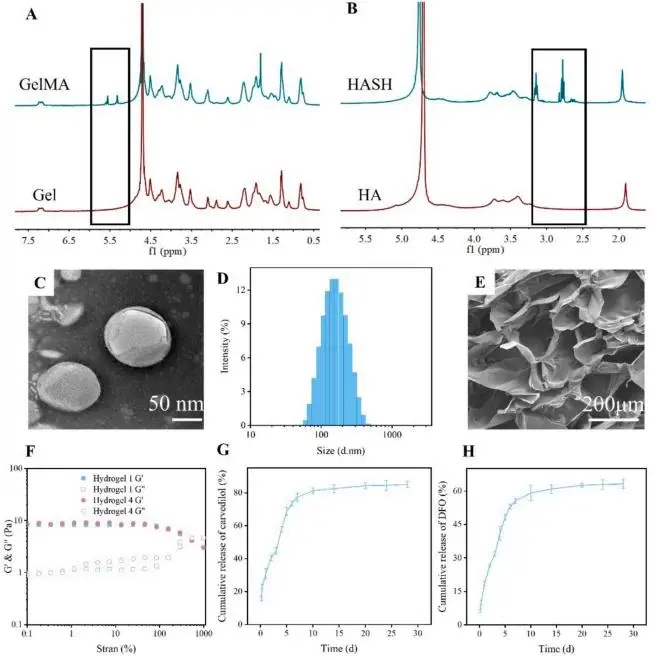
图1.(A)Gel,GelMA和(B)HA,HASH的1H NMR。(C)DPDCN的TEM图像(比例尺:100 μm)。(D)DPDCN的粒度分布。(E)水凝胶4的SEM图像(比例尺:(F).水凝胶振幅扫描试验。以恒定频率(1Hz)进行测量。(G)卡维地洛和(G)在37 ℃下从PBS中的水凝胶4的DFO释放速率
(2)水凝胶的体外ROS清除和抗炎活性
在H₂O₂诱导的H9C2氧化应激模型中,图S14系统评价了DPDCNs浓度-效应关系:0–50 μg/mL范围内细胞活性随剂量递增,于50 μg/mL达峰值(约为H₂O₂组的1.8倍),继续升高至100 μg/mL则出现轻度回落,提示最适负载量;所有含DPDCNs水凝胶组活性均显著高于单纯H₂O₂损伤组,奠定后续实验剂量基础。ROS检测方面,图2A与S15的DCFH-DA荧光成像显示,含卡维地洛的Gel-3、Gel-4组绿色信号较H₂O₂组分别降低62 %与71 %;图S16定量结果进一步证实,Gel-4组胞内ROS水平降至对照组的38 %,显示出剂量-依赖的自由基清除能力。凋亡实验图2B Annexin V-FITC/PI双染流式结果显示,Gel-4干预后早期凋亡率由H₂O₂组的28.7 %降至9.4 %,晚期凋亡+坏死率由15.2 %降至4.1 %,总体存活率提升至86.5 %,表明其可显著抑制氧化应激触发的细胞凋亡与坏死。
抗炎评价采用LPS激活的RAW264.7巨噬细胞模型。细胞因子谱方面,图2D-E的ELISA结果表明,LPS刺激48 h后TNF-α与IL-6分别高达295.7 pg/mL与113.3 pg/mL,而Gel-4组将二者分别抑制至108.2 pg/mL与41.6 pg/mL,抑制率分别为63 %与63.3 %;图2C免疫荧光与图S18定量统计进一步证实,TNF-α蛋白红色荧光强度下降68 %。与之对应,图2F显示抗炎因子IL-10在Gel-4组升高至37.4 pg/mL,较LPS组提升40 %,综合表明Gel-4通过下调促炎因子、上调抑炎因子并促进M2极化,实现显著的体外抗炎效应,为其用于心肌梗死后期炎症调控提供实验依据。
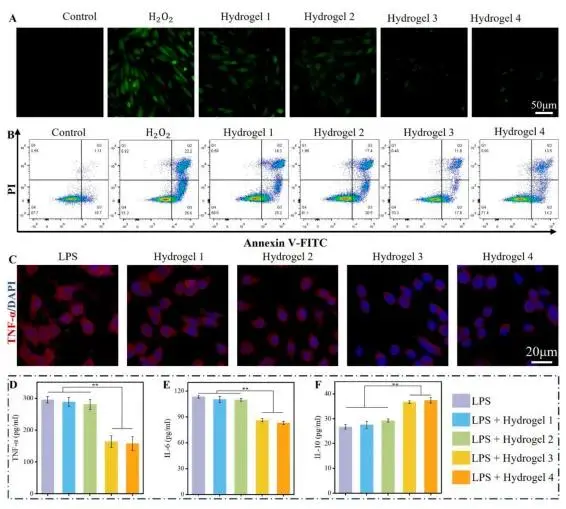
图2. (A)H2O2处理48 h H9C2 的ROS染色;(B) H2O2和不同水凝胶样品处理48小时的H9C2细胞的膜联蛋白V-FITC/PI双染色流式细胞术结果,坏死细胞(Annexin-V/PI − /+;左上);凋亡细胞(Annexin-V/PI +/+和Annexin-V/PI +/− ;右上和右下);活细胞(Annexin-V/PI − /− ;左下);(C)LPS刺激48 h RAW264.7 TNF-α免疫荧光;(D−F)该条件下IL-6、TNF-α、IL-10水平
(3)多功能水凝胶对内皮细胞迁移和管腔形成的影响
在24 h划痕实验中,图3A直观显示含DFO的Gel-2与Gel-4组HUVEC迁移面积已覆盖约75 %的初始划痕区,而无DFO的Gel-1与Gel-3组仅修复约35 %,差异具有统计学显著性;至36 h,Gel-4组划痕基本闭合,剩余缺口宽度不足起始的10 %,对照组与无DFO组仍保留30 %以上未愈合区域。图3C的定量分析进一步证实,Gel-4组的迁移/增殖速率较对照提升约2.1倍,显著高于其他实验组。管腔形成实验方面,图3B的6 h荧光图像可见Gel-4组已出现密集且连续的多边形血管网,节点数、分支点及总管长均显著增加;图3D-E统计显示,其节点数达到每视野48 ± 5个,分支点41 ± 4个,总管长为4.8 ± 0.3 mm,分别约为对照组的2.5倍、2.3倍和2.6倍,且无DFO组未见显著差异,充分说明DFO负载的水凝胶通过协同促进内皮细胞迁移与管腔结构化,显著加速体外血管新生过程。
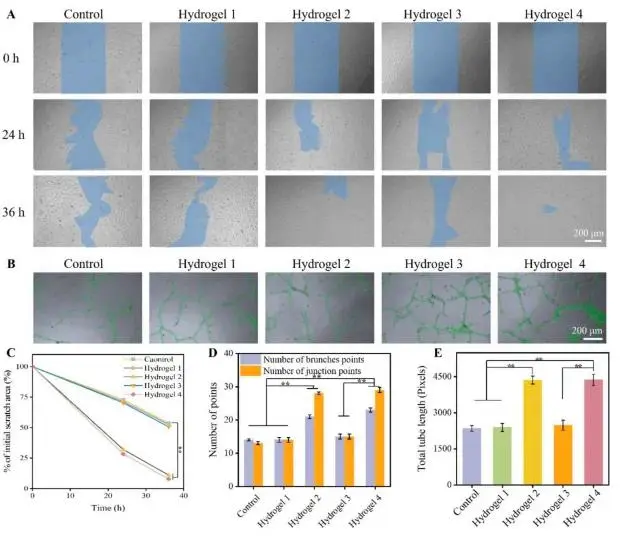
图3. (A)HUVEC划痕0、24、36 h图像;(B)体外管腔形成图像;比例尺200 μm;(C)划痕愈合率(n=3);(D)节点数、分支点数;(E)总管长度
(4)多功能水凝胶体内抗氧化、抗凋亡作用及体内抗炎作用评价
图4A的活体ROS成像显示,术后3 d MI组梗死区绿色荧光信号强度约为Sham组的3.4倍,提示氧化应激剧增;Gel-4组荧光强度降至Sham组的1.1倍,显著低于其余各治疗组,证实其清除ROS能力最优。图4G定量统计进一步验证,Gel-4组相对荧光强度较MI组下降67 %,且差异具有统计学意义(p < 0.001)。图4B的TUNEL染色显示,MI组凋亡阳性细胞率高达38.5 %,Gel-4组降至9.2 %,为各组最低;图4H定量分析表明,其凋亡抑制率约为76 %,显著优于Gel-3组(抑制率52 %),显示清除ROS后有效阻断心肌细胞凋亡。炎症因子检测方面,图4E的ELISA结果显示,Gel-4组梗死区IL-1β浓度为85 pg/mg蛋白,较MI组(210 pg/mg蛋白)降低59 %;图4F显示TNF-α水平由MI组的312 pg/mg蛋白降至Gel-4组的118 pg/mg蛋白,降幅达62 %,均显著低于其余水凝胶治疗组。巨噬细胞表型分析中,图4C免疫荧光显示,Gel-4组CD86(M1标志)阳性面积占梗死区5.1 %,显著低于MI组的21.3 %;图4D显示CD206(M2标志)阳性面积升至28.7 %,为MI组的2.9倍,提示Gel-4有效促进M1向M2型极化,协同抑制炎症并推动心肌修复进程。

图4. 治疗后3 d水凝胶抗氧化、抗凋亡及抗炎评估:代表性图像(A)ROS(红)、(B)TUNEL(绿)、(C)CD206(绿)、(D)CD86(红)、(E)TNF-α(绿)、(F)IL-1β(绿)荧光图及(G-L)对应定量分析
(5)多功能水凝胶的体内治疗效果评价
图5A-E的超声参数显示,14 d时MI组左心室扩张明显,EDV与ESV分别达1.44 ± 0.08 mL和0.73 ± 0.05 mL,EF、FS分别降至45.4 ± 2.1 %与19.7 ± 1.3 %;Gel-4组EDV、ESV分别被抑制至0.96 ± 0.06 mL和0.38 ± 0.03 mL,EF、FS回升至65.8 ± 3.2 %与32.4 ± 2.0 %,显著优于其余治疗组。至28 d,Gel-4组EF进一步升至78.9 ± 2.5 %,FS达45.6 ± 1.8 %,接近Sham组水平(EF 82.1 %、FS 48.3 %),证实其持续改善收缩功能。图5F H&E显示Gel-4梗死壁厚度增至1.28 ± 0.09 mm,较MI组提升76 %;Masson染色示胶原面积分数由MI组的41.3 %降至13.7 %,纤维化显著减轻。
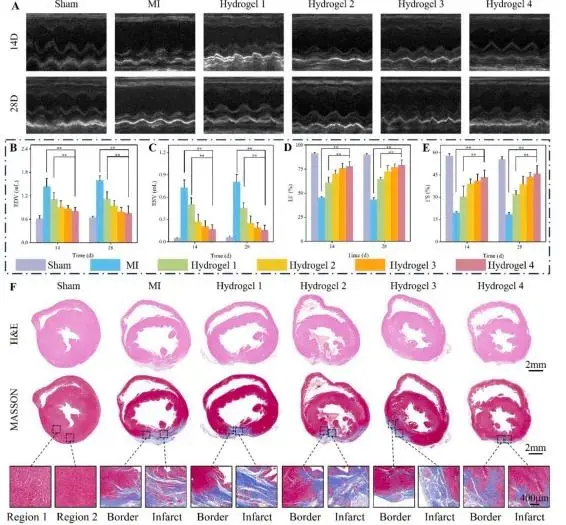
图5. 水凝胶治疗后大鼠心功能与心室重塑评估:(A)第14、28天各组超声心动图;(B-E)EF、FS、ESV、EDV统计;(F)28天梗死心脏H&E与Masson染色
(6)多功能水凝胶体内血管生成作用和心脏功能影响的评价
图6A–B的免疫荧光显示,28 d时Gel-4组梗死边缘区VEGF阳性面积占(39.8 ± 3.1)%,HIF-1α阳性面积占(42.5 ± 2.7)%,分别为MI组的3.2倍与3.4倍,且显著高于Gel-2组(VEGF 24.6 %、HIF-1α 26.3 %),证实DFO持续激活HIF-1α/VEGF轴并促进血管新生;图6E–F定量荧光强度亦呈相同趋势,Gel-4组VEGF、HIF-1α强度较MI组提升约2.9倍与3.1倍。心肌结构蛋白方面,图6C、G显示α-actinin在Gel-4组荧光强度为(18.7 ± 1.3)×10³ a.u.,较MI组提高了2.5倍,表明肌节成熟与收缩单元恢复;图6D、H显示CX43在Gel-4组表达量达(21.4 ± 1.8)×103 a.u.,为MI组的4.3倍,缝隙连接重构显著,电-收缩耦联功能明显改善。综合图6结果,Gel-4通过协同促血管新生、抑制炎症及氧化应激,最终实现心肌结构修复与功能恢复。

图6.28天水凝胶促血管与心肌修复:(A)VEGF(绿)、(B)HIF-1α(绿)、(C)α-actinin(红)、(D)CX43(绿)免疫荧光及(E-H)平均荧光强度统计
本研究构建的GelMA/HASH@DPDCNs可注射水凝胶兼具良好生物相容性与多重治疗功能:体外促进HUVEC迁移成管,减轻H2O2诱导的H9C2凋亡,并驱动巨噬细胞M2极化、抑制炎症因子;大鼠MI模型中,通过促血管新生、抗氧化与抗炎协同作用显著改善心功能、缩小心梗面积并增加室壁厚度。尽管机制细节及大动物验证仍需深入,该凝胶为MI微创联合治疗提供了新策略。

|
创赛生物 提供高品质的医疗产品和服务 |
联系我们 |
产品中心 |
扫码关注
关注公众号 扫码加客服
|

