
心肌梗死(MI)是缺血性心血管疾病的主要形式,严重威胁着人类的健康。心肌梗死后,血氧供应的突然停止导致代谢变化和心肌凋亡,进一步激活心肌的炎症反应和纤维化,增加心力衰竭的发生概率。阻断缺氧诱导的不良反应对心肌梗死后心功能的恢复具有潜在的作用。缺氧条件下心肌保护的基础是增加缺氧诱导因子-1α(HIF-1α)的表达水平。HIF-1α的高表达可改善细胞凋亡,抑制炎症反应,抑制纤维化促进梗死后组织修复。HIF-1α(hypoxia induced factor-1α)是心肌梗死(MI)后重要的缺氧保护信号,其生存期较短。通过使用脯氨酸羟化酶抑制剂如DPCA(1,4-二氢phenonthrolin-4- 1 -3-羧酸)抑制HIF-1α的羟基化作用来提高HIF-1α的稳定性,结果是积极的。但是,游离的DPCA分子量小,溶解度差,导致其体内半衰期短,因此限制了HIF-1的稳定性和对DPCA治疗MI的理想释放谱的研究。

针对上述问题,浙江大学朱旸、任探琛、高长有教授团队设计和合成了可注射的热敏水凝胶,具有可编程的DPCA释放。水凝胶降解和缓慢的DPCA释放耦合形成一个反馈回路,通过将悬垂的DPCA附着在聚合物骨架上,通过Π-Π和疏水相互作用作为额外的交联点。悬垂羧基被添加到共聚物中以加速DPCA的释放。急性期为心肌保护作用的突发释放和不同速率的炎症期和纤维化期的近零级延长释放。所有释放DPCA的水凝胶上调HIF-1α,减少细胞凋亡,促进血管生成,刺激心肌细胞增殖,从而保持心功能和心室几何形状。更快的DPCA释放导致更快的水凝胶降解导致HIF-1α表达量是健康对照组的8倍,并且在心肌梗死治疗中效果更好。本研究证实了精确调控HIF-1α表达在治疗心肌梗死等相关疾病中的价值,并提供了一种基于植入式装置的调控策略。该文章于2024年09月23日以《Thermosensitive Hydrogel with Programmable, Self-Regulated HIF-1α Stabilizer Release for Myocardial Infarction Treatment》为题发表于《Advanced Science》(DOI:10.1002/advs.202408013)。
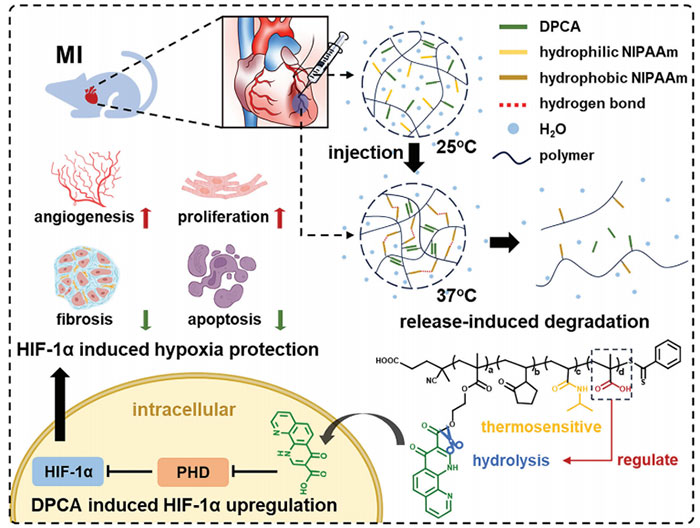
图1. 可注射释放降解热敏水凝胶稳定心肌梗死HIF-1α的设计、功能及应用
(1) DPCA系链聚合物的合成与表征
研究人员通过两步可逆加成-断裂链转移(RAFT)聚合法成功合成了含DPCA接枝的聚合物PNVH和聚合物PNVMH(图2A)。通过活化DPCA,将其羧基转化为咪唑啉基团,并通过1H NMR光谱验证这一过程,显示羧基氢消失及苯环区域新峰的出现。实验通过监测1H NMR光谱中的特征峰变化,确认了聚合过程的成功(图2B),同时计算和验证了单体的聚合度(表1)。最后,通过在HEMA羟基上接枝DPCA,合成了PNVD和PNVMD,进一步通过NMR光谱证实了这一点。
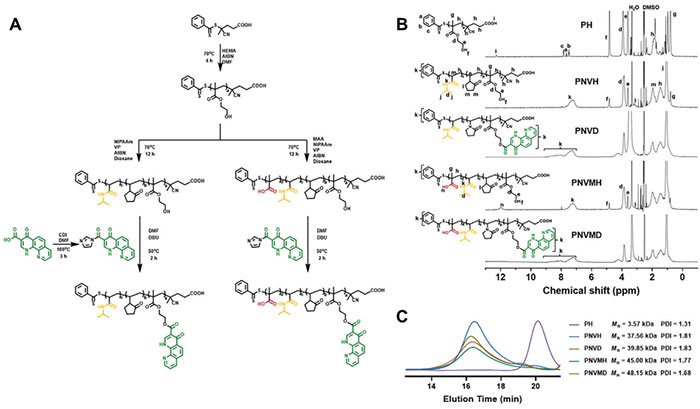
图2. A) PNVD 和 PNVMD 的合成路线;B) 聚合物及其中间体的 1H NMR;C) 使用 HFIP 作为洗脱液的 SEC 分析聚合物及其中间体的痕迹
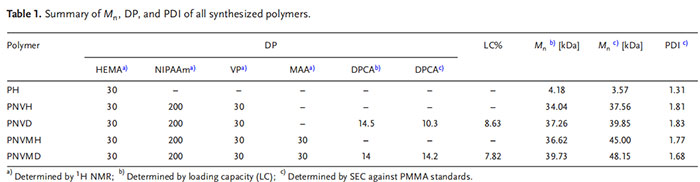
表1. 所有合成聚合物的Mn、DP和PDI
(2) 负载DPCA的热敏水凝胶的性能
研究人员通过动态光散射和流变学分析测量了不同聚合物的低临界溶解温度(LCST),并发现PNVD在37 ℃时表现出明显的溶胶-凝胶转变,其水合直径从49.56 nm减小至13.63 nm,表明疏水相互作用导致聚合物链收缩(图3A和3B)。相比之下,PNVMD在整个温度范围内保持稳定的凝胶状态,如图3C所示,PNVD的G'和G"在≈35 ℃时显著增加,且G'超过G",表明溶液发生了溶胶-凝胶转变。相比之下,PNVMD的G'和G"随温度变化较小,且在整个测试温度范围内G'始终大于G",表明PNVMD保持凝胶状态。这种差异归因于PNVMD的强分子间相互作用和聚合物拓扑结构,为热敏材料的研究提供新思路,DPCA是一种稳定HIF-1α的PHDs抑制剂,其释放特性在缺血环境中对治疗效果至关重要。此外,研究结果显示,水凝胶在前3天内释放物理结合的DPCA,随后共价结合的DPCA随聚合物降解逐渐释放(图3D-F)。MAA的引入加速了酯水解,提升了PNVMD的整体释放速率,使其在21天内几乎全部释放DPCA,而PNVD则低于50%。更有趣的是,PNVD和PNVMD在不同阶段表现出近似零级释放,这源于聚合物结构的独特设计(图3G)。这种智能控制的释放方式为心肌修复等应用提供了新的研究方向。
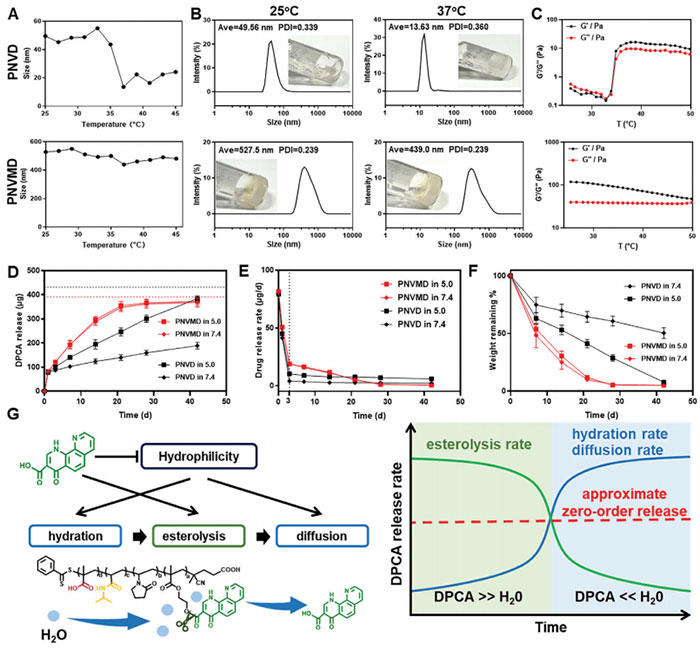
图3. A) 在浓度为 1 mg·mL⁻¹ 时,通过 DLS 测量温度诱导的 PNVD 和 PNVMD 的 LCST(PNVD 的 LCST 为 ≈35 ℃,PNVMD 无显著 LCST);B) 在 25 ℃ 和 37 ℃ 时,PNVD 和 PNVMD 水凝胶(1 mg·mL⁻¹)的粒径分布;C) 不同温度下 PNVD 和 PNVMD 水凝胶的流变性能;D) 在 pH 7.4 和 5.0 时,PNVD 和 PNVMD 的累积药物释放量。红色和黑色虚线分别表示 PNVD 和 PNVMD 的理论载药量(n = 4);E) pH 为 7.4 和 5.0 时,PNVD 和 PNVMD 的药物释放率(n = 4);F) 在 pH 7.4 和 5.0 下 PNVD 和 PNVMD 的降解(n = 4)。数据以 mean ± SD 表示;G) 共价键 DPCA 的近似零级释放示意图
(3) 程序化DPCA释放水凝胶用于改善心功能
研究人员引入PNVH作为无药对照组,由于PNVH的成分和性质与PNVH相似,未纳入PNVH。研究结果显示,在第7天,作为心功能评估关键指标的LVEF在MI组(46.65%)明显低于Sham组(94.98%),表明心肌梗死后心功能不全。此时,PNVD组显著提高了LVEF(63.66%),而PNVH和PNVD组由于机械作用和药物释放有限,没有表现出明显的改善心功能的能力。28 d后,未进行水凝胶干预的梗死心肌(MI组,28 d)进一步恶化,LVEF降至39.53%。水凝胶治疗对心功能有改善作用,反映在LVEF上。PNVH组LVEF(47.41%)略高于MI组。PNVD组对高LVEF的心功能改善较好(55.48%)。与PNVD组相比,PNVMD组LVEF明显升高达到73.99%(图4A-C),显示出DPCA的快速释放在增强心脏功能中的潜力。
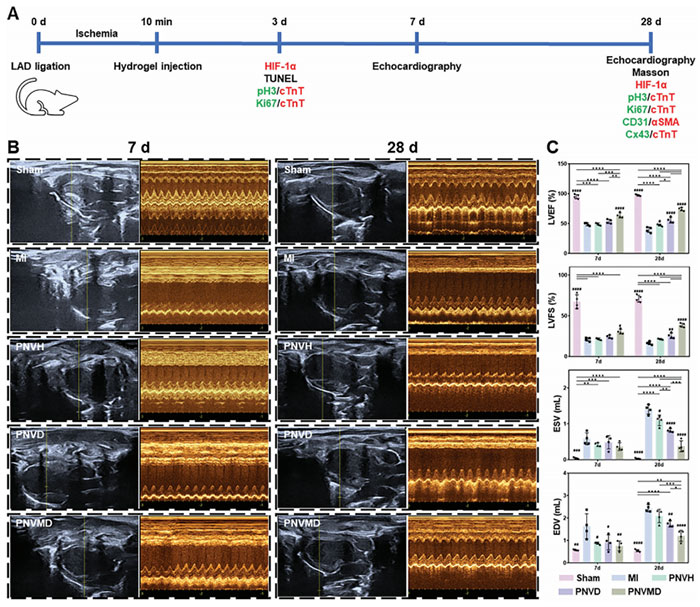
图4. A) 动物实验时间表。假手术组(行开胸手术,未结扎 LAD);MI 组(LAD 结扎 + 盐水注射);PNVH 组(LAD 结扎 + PNVH 水凝胶注射);PNVD 组(LAD 结扎 + PNVD 水凝胶注射);PNVMD 组(LAD 结扎 + PNVMD 水凝胶注射);B) 各组分别在 7 d 和 28 d 的代表性超声心动图;C) 基于 (B) 的 LVEF、LVFS、ESV 和 EDV 的统计值
(4) 水凝胶对 HIF-1α 诱导的心肌细胞凋亡和再生的影响心肌细胞凋亡和再生的影响
DPCA上调的HIF-1α表达在心肌梗死(MI)治疗中的再生和抗凋亡效果显著。PNVD和PNVMD组的HIF-1α表达在MI后第3天显著增加(图5),特别是PNVMD组的快速DPCA释放效果最佳。DPCA诱导的HIF-1α上调降低了心肌细胞凋亡比例,使PNVMD组的细胞凋亡降至11.84%,明显优于其他组。此外,水凝胶治疗提升了关键蛋白Cx43和cTnT的表达,促进了心肌功能恢复。实验进一步证实,HIF-1α上调能促进缺血心肌中pH3和Ki67的表达,助力细胞增殖,为MI后的心肌再生提供了新思路。
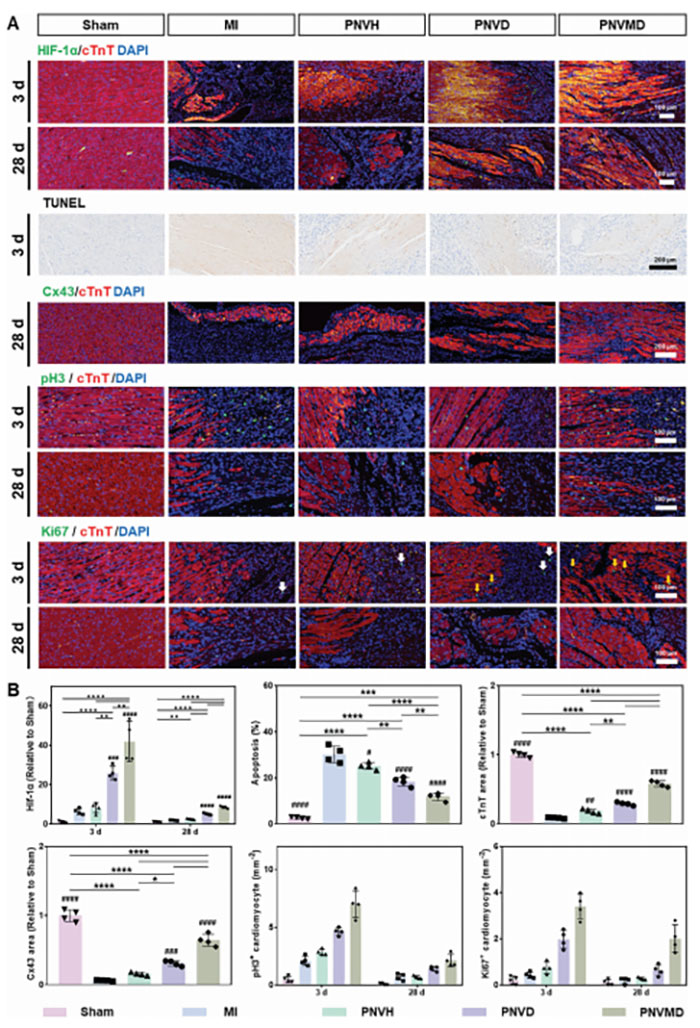
图5. A) 水凝胶治疗 3 天和 28 天后心脏切片的组织学评估:代表性免疫荧光染色图像显示 HIF-1α(绿色)、cTnT(红色)和细胞核(蓝色)(3 天和 28 天);代表性 TUNEL 染色图像(仅 3 天);代表性免疫荧光染色图像显示 Cx43(绿色)、cTnT(红色)和细胞核(蓝色)(仅 28 天);代表性免疫荧光染色图像显示 pH3(绿色)、cTnT(红色)和细胞核(蓝色)(3 天和 28 天);代表性免疫荧光染色图像显示 Ki67(绿色)、cTnT(红色)和细胞核(蓝色)(3 天和 28 天)。白色和黄色箭头分别代表纤维细胞和心肌细胞中的阳性标记。B) 基于 (A) 中相应的免疫荧光染色图像和 TUNEL 染色图像,对 HIF-1α 表达、凋亡、cTnT 表达、Cx43 表达、pH3 表达和 Ki67 表达的定量分析
(5) 程序化DPCA释放水凝胶通过减少纤维化和血管化治疗心肌梗死
研究人员在心肌梗死后28 d使用马松三色染色检测纤维化,Masson三色染色实验结果显示,DPCA干预能显著减少心肌纤维化,PNVMD组纤维化最少,仅为10.39%,优于其他实验组(图6)。PNVD组显示了较慢的水凝胶降解,这与体外实验结果一致。此外,CD31和α-SMA染色结果显示,在Sham组中,观察到极少的新血管,而在MI和PNVH组中存在许多血管。这可能是由于心肌启动的自我防御机制,通过诱导血管再生来抵消梗死部位缺血缺氧微环境。PNVMD组具有最高的血管再生密度,说明DPCA的合理释放与机械支撑能显著促进血管再生,为心肌修复提供了强有力的支持。
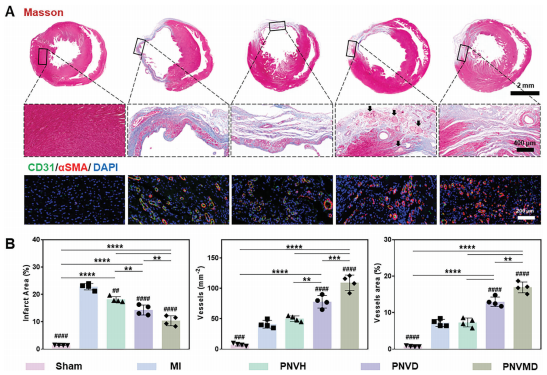
图6.A)水凝胶治疗效果的组织学评价:心脏切片CD31(绿色)、α-SMA(红色)和细胞核(蓝色)的代表性马松三色染色和代表性免疫荧光染色图像; B) 基于(A)中的Masson三色染色和相应的免疫荧光染色图像,对梗死面积和血管化的定量分析
研究小结:
为了探索心肌梗死后HIF-1α的表达是否稳定和调节,我们设计了PNVD和PNVMD水凝胶,这些水凝胶能够可编程释放HIF-1α的稳定剂。通过调节连接到聚合物主链的DPCA的酯键水解和游离DPCA的扩散之间的相互作用,我们在急性期实现了快速释放,在炎症和纤维化期实现了长时间的近零级释放,释放速率不同。局部释放的DPCA通过上调HIF-1α,减少细胞凋亡,促进血管生成和刺激心肌细胞增殖来维持心功能和心室几何形状。PNVMD的DPCA释放速度比PNVD快,导致心肌组织中HIF-1α的水平更高,达到健康基线的8倍,从而产生优越的治疗效果。综上所述,本工作为心肌梗死治疗中HIF-1α的表达调控指明了优化方向,提供了一种基于水凝胶的调控方法。

|
创赛生物 提供高品质的医疗产品和服务 |
联系我们 |
产品中心 |
扫码关注
关注公众号 扫码加客服
|

